Organizado por el IRB Barcelona en colaboración con la Fundació Catalunya – La Pedrera.
Los tutores de esta edición son: Jesús Herráiz, Sylwia Gawrzak, Salvador Pérez, Bahareh Eftekharzdeh, Berta Terré, Paula Martínez-Cristóbal, Carlos Maíllo Carbajo, Julia García, Antonija Kuzmanic, Arturo Rodríguez-Banqueri, Joana Raquel Faria y Mohammed Rahman.
Presentation

Participantes del curso “Crazy About Biomedicine”, edición 2015.
Objetivos
Bojos per la Biomedicina és un curs d'un any de durada dirigit als estudiants del primer any de batxillerat que desitgin explorar alguns dels descobriments fascinants que s'estan fent actualment en les ciències de la vida. A través d'aquest curs, els estudiants tindran l'oportunitat d'aprofundir el seu coneixement de la teoria i tècniques científiques en el camp de la biomedicina. Treballaran juntament amb investigadors joves per experimentar com es fa ciència en un institut de recerca internacional, guanyar una mica d'experiència pràctica en les últimes metodologies d'avantguarda i posicionar-se per a una possible carrera professional en les ciències de la vida.
Descripción del curso
Aquest curs combina sessions teòriques i activitats experimentals pràctiques, que es duran a terme durant 18 dissabtes de l'any. El curs tractarà 12 temes científics actuals, que van des de la biologia cel·lular i molecular fins a la biologia estructural i computacional i la química, presentats per estudiants de doctorat de l'IRB Barcelona. En el primer «semestre» (gener-juny 2015), els 3 primers dissabtes es dedicaran a aquestes sessions teòriques generals per a tots els participants. Durant els 6 dissabtes següents, es formaran grups petits que entraran als laboratoris per a les sessions pràctiques. A continuació, es repetirà aquest programa amb 6 temes de recerca nous per al segon semestre (juny-desembre). Els estudiants participants s'hauran de comprometre a assistir al curs durant tot l'any.
Idioma del curso
Totes les xerrades i sessions pràctiques es faran en anglès.
Fechas y horarios
El curs es farà de gener a desembre de 2015, 10.00h-14.00h
SEMESTER I
- Divendres, 9 de gener: Inauguració al Mon Sant Benet –Sant Fruitós del Bages
- Dissabte, 17 de gener: Seminari 1
- Dissabte, 31 de gener: Seminari 2
- Dissabte, 7 de febrer: Seminari 3
- Dissabte, 21 de febrer: Tallers 1
- Dissabte, 7 de març: Tallers 2
- Dissabte, 21 de març: Tallers 3
- Dissabte, 11 d’abril: Tallers 6
- Dissabte, 25 d’abril: Tallers 4
- Dissabte, 9 de maig: Tallers 5
SEMESTER II
- Dissabte, 23 de maig: Seminari 1
- Dissabte, 30 de maig: Seminari 2
- Dissabte, 13 de juny: Seminari 3
- Dissabte, 19 de setembre: Tallers 1
- Dissabte, 3 d’octubre: Tallers 2
- Dissabte, 17 d’octubre: Tallers 3
- Dissabte, 31 d’octubre: Tallers 4
- Dissabte, 14 de novembre: Tallers 5
- Dissabte, 28 de novembre: Tallers 6
- Dissabte, 10 de gener de 2016: Cerimonia de cloenda
Precio del curso
Les despeses de l’acció formativa corren a càrrec de la Fundació Catalunya-La Pedrera. Tot i això els participants abonaran 120 euros corresponent a les despeses d’organització i gestió del programa. No s'inclouen dinars ni esmorzars. Els estudiants rebran un certificat de participació en finalitzar el curs amb èxit en una cerimònia especial de cloenda.
Lugar de celebración
Insitut de Recerca Biomèdica (IRB Barcelona)
c/ Baldiri Reixac, 10
Barcelona
Quién puede solicitar una plaza
Aquest curs està dirigit als estudiants de primer any de batxillerat que tinguin un interès i talent especials en els camps relacionats amb les ciències de la vida (principalment biologia i química).
Els estudiants poden sol·licitar la plaça a un màxim de 2 dels programes de la série "Bojos per la Ciència" i participar només en un.
Cómo solicitar la plaza
Els estudiants interessats hauran d'emplenar el formulari web de sol·licitud i incloure una carta de motivació. També es demanarà una carta de recomanació directament de dos dels seus professors que la coneguin bé. En el cas de que l'estudiant hagi canviat de centre aquest curs, suggerim que sol·licitin les cartes als antics professors. La data límit d'inscripció és el 14 October 2013.
El curs està obert a un total de 24 estudiants. Se seleccionaran els candidats en funció del seu expedient acadèmic, de les recomanacions dels seus professors i de la seva motivació per participar-hi. Es convidarà els candidats preseleccionats a fer entrevistes amb els organitzadors científics al novembre, després de les quals es farà la selecció final. La primera setmana de desembre es comunicarà el resultat als estudiants. Es demanarà als estudiants seleccionats per participar-hi i als seus pares/tutors legals que signin una carta de compromís d'assistir a totes les sessions.
Fechas importantes
- 14 d’octubre de 2014: Data límit d'inscripció
- Setmana del 3 de novembre de 2014: Contacte amb els candidats preseleccionats
- 19-28 de novembre de 2014: Entrevistes
- 1-5 de desembre de 2014: Publicació del llistat dels estudiants acceptats
- Dissabte, 9 de gener de 2015: Inauguració a La Pedrera
- Dissabte, 16 de gener de 2015: Inici del curs
Colaboradores
Fundació Catalunya La Pedrera, Parc Científic de Barcelona



Si tienes alguna pregunta, contactanos en: irb_outreach@irbbarcelona.org
Programme
SEMESTRE 1
1. Estan lligades l’apoptosi i/o la proliferació cel·lular amb un increment de la malignitat tumoral?
Nuno Vasconcelos (Servei d’Histologia)
Les alteracions en la proliferació i l’apoptosi cel·lulars són fonamentals en els primers esdeveniments tumorals, alhora que són útils per caracteritzar quin teixit és histològicament normal i quin té un creixement tumoral. Aquí, intentarem entendre si una simple caracterització de teixits normals i tumorals amb marcadors d’apoptosi i proliferació són suficients per diferenciar un càncer altament maligne d’altres tipus de càncer.
Aquest curs donarà una visió general de les tècniques histològiques alhora que tractarà diferents aspectes del càncer. Intentarem determinar si alguns marcadors proteics (i.e. ki67, caspasa-3, entre d’altres) mostren expressió diferencial al llarg dels diferents estadis d’un tipus de càncer. La part teòrica estarà il·lustrada per diferents exemples de tècniques experimentals. Durant la part pràctica, durem a terme tincions histològiques (Hematoxilina/eosina, tricromat de Masson) i compararem diferents tipus de mostres de teixit de ratolí per identificar diferents proteïnes i teixits.
2. Una visió general de la metàstasi: Com les cèl·lules envaeixen teixits distants?
Sylwia Gawrzak (Gomis Lab)
La Metàstasi és un procés complex i amb diferents passos en el qual les cèl·lules cancerígenes deixen el tumor original i migren cap a altres parts del cos principalment mitjançant el corrent sanguini. La recaiguda metastàtica és un esdeveniment tardà, associat amb un mal pronòstic de la progressió cancerígena i està relacionat amb la letalitat del càncer. Tot i que les estratègies per atacar els tumors primaris han millorat, els tractaments per prevenir la metàstasi són molt menys efectius. Conseqüentment, la metàstasi roman com un repte clínic, i la dissecció dels seus mecanismes biològics és crucial per trobar dianes terapèutiques per prevenir i curar els tumors malignes.
Aquest curs donarà una visió general de la biologia del càncer amb un enfoc especial als diferents aspectes de la metàstasi. Aprendrem on les cèl·lules cancerígenes formen metàstasi, els passos essencials en el procés i quant temps és necessari per a que es dugui a terme. La part teòrica estarà acompanyada de diferents exemples de tècniques experimentals per estudiar la metàstasi. Durant la part pràctica, farem diverses tincions histològiques i compararem diverses mostres de teixit de ratolí per identificar lesions metastàtiques en diferents òrgans.
3. Un codi que marca el desenvolupament
Salvador Pérez (Azorín Lab)
L’ADN eucariota no està nu sinó que es troba organitzat en una estructura anomenada cromatina, formada per subunitats anomenades nucleosomes. Un nucleosoma és una estructura formada per quatre proteïnes anomenades histones que formen un nucli central on el ADN s’hi enrotlla al voltant. Durant els últims anys, el nostre coneixement sobre la regulació i la funció de la cromatina ha millorat molt gràcies a la identificació de nombroses modificacions en les histones, variants de les histones, complexos remodeladors i altres proteïnes estructurals i no-estructurals. Aquests factors tenen un paper en la compactació de la cromatina i això comporta canvis en la expressió gènica. L’epigenètica estudia com aquests factors afecten l’expressió gènica i la seva importància durant el desenvolupament i altres processos cel·lulars com la replicació, la transcripció i d’altres.
El nostre grup estudia les bases moleculars de l’estructura de la cromatina, així com la funció i la seva regulació durant el cicle cel·lular i el desenvolupament de l’organisme. Utilitzem Drosophila melanogaster (la mosca del vinagre) com a organisme model. En aquest curs veuràs com el nostre desenvolupament té moltes similituds amb el de les mosques.
Durant el curs estudiarem una de les proteïnes que s’uneix al ADN i que participa en la organització de la cromatina. Ens centrarem en una de les variants de la histona H1 i algunes de les seves modificacions per entendre com aquestes proteïnes afecten l’expressió gènica i el desenvolupament de Drosophila.
4. Introducció a la neurodegeneració i les malalties neurodegeneratives.
Bahareh Eftekharzdeh (Salvatella lab)
L’Alzheimer és la forma més comú de demència senil. Actualment no té cura i els seus símptomes empitjoren amb la progressió de la malaltia, portant cap a la mort del malalt. Va ser descrita per primer cop per un neuropatòleg i psiquiatre alemany, Alois Alzheimer al 1906. Les causes i la progressió de la malaltia encara no són del tot enteses. La investigació indica que la malaltia està associada amb plaques al cervell. Els tractaments actuals només ajuden a pal·liar els símptomes però no aturen o inverteixen el procés degeneratiu. Al 2012, més de 1000 assajos clínics estaven en marxa per trobar una cura per l’Alzheimer, encara no es coneix si cap d’aquests tractaments serà efectiu. L’estimulació mental, l’exercici, i una dieta equilibrada semblen retardar els símptomes cognitius (però no la degeneració del cervell) en pacients d’avançada edat, tot i això no hi ha unanimitat en el seu efecte. Aquest curs tractarà els mecanismes de la neurodegeneració, amb especial èmfasi en l’Alzheimer i el Parkinson.
El curs començarà amb una introducció a la història d’aquestes dues malalties, des que van ser examinats els primers cervells de pacients fins l’actualitat. Seguirem amb una explicació dels mecanismes cel·lulars i moleculars de la malaltia. Continuarem amb algunes de les hipòtesis per a la seva causes, i els avenços més recents per trobar una cura, incloent les estratègies clíniques més innovadores. Finalment, tindrem una sessió de preguntes on els estudiants tindran l’oportunitat de pensar estratègies d’investigació en aquest àmbit mirant al futur.
5. Entenent l’ADN: Que et fa a tu diferent de la resta?
Berta Terré (Stracker Lab)
Es pot dir que l’ADN és el manual d’instruccions genètic de les nostres cèl·lules. Aquesta molècula conté la informació genètica que controla totes les funcions cel·lulars com la proliferació o l’apoptosi, o altres processos més complexes com el color dels nostres ulls. Tot i això, l’ADN pot patir alteracions que afectin aquests processos duent a processos patològics com el càncer. Per això les nostres cèl·lules han desenvolupat mecanismes de control per reparar tots els errors que puguin ocórrer a l’ADN, el que s’anomena via de resposta als danys a l’ADN. Es a dir, tenim certs gens, la funció dels quals és la de protegir el genoma, són responsables de mantenir l’estabilitat genòmica i protegir les nostres cèl·lules. Malgrat això, aquest sistema no actua igual per tothom iésper això que tot i tenir estils de vida similars algunes persones desenvolupin càncer i altres no.
En aquest curs, explorarem la relació entre la inestabilitat genòmica (canvis a l’ADN) i el càncer. Intentarem entendre els mecanismes pels quals l’ADN controla les funcions cel·lulars i com les diferències genètiques que existeixen entre nosaltres influencien en el risc de patir càncer.
Aquest curs continua al segon semestre.
6. Com els mitocondris es mouen… i maten
Paula Martínez-Cristóbal (Zorzano Lab)
Els mitocondris són orgànuls mòbils que existeixen en xarxes dinàmiques. Contínuament s’uneixen en processos de fusió i es divideixen per processos de fissió. El secret de la seva dinàmica esta sent revelat gràcies a la microscòpia confocal, la imatge en viu i la utilització de proteïnes que marquen els mitocondris.
La fusió i fissió dels mitocondris controlen processos cel·lulars bàsics com la homeòstasi del càncer i la generació d’ATP i radicals d’oxigen i conseqüentment tenen un paper important paper en el cicle cel·lular, l’apoptosi, la mitofàgia i la detecció d’oxigen. Per això, alteracions en la dinàmica dels mitocondris contribueix a la patogènia de malalties complexes en les quals els mitocondris no han estat involucrats anteriorment; aquestes malalties inclouen el càncer, malalties cardiovasculars i malalties neurodegeneratives.
En aquest curs, veurem la relació entre la dinàmica dels mitocondris, l’apoptosi i l’autofàgia. Els estudiants faran diferents experiments amb cèl·lules i treballaran per entendre el paper de algunes proteïnes mitocondrials que participen en la fusió mitocondrial.
SEMESTRE 2
1. Observem de ben a prop els pèptids
Jesús Herráiz (Albericio Lab)
Les proteïnes són gran molècules complexes que participen en múltiples processos en el nostre cos. Fan la majoria de la feina a les cèl·lules i són essencials per la correcta funció, defensa i senyalització als nostres teixits i òrgans. Entendre la seva estructura ens ajuda a entendre millor la seva funció i les seves interaccions.
Químicament, les proteïnes són biomolècules que estan formades per una o més cadenes d’aminoàcids. Una cadena linear d’aminoàcids és coneguda com a polipèptid. Una proteïna conté com a mínim una cadena llarga polipeptídica. Els polipèptids curts, els que contenen entre 20-30 aminoàcids són coneguts com a pèptids. Treballar amb pèptids és complex de degut a la seva petita mida.
En aquest curs veurem alguns dels mètodes actuals que s’utilitzen en la recerca amb pèptids.
2. Dissenyant medicaments amb pèptids
Júlia Garcia (Giralt Lab)
Els pèptids són petites proteïnes fetes d’un número petit d’aminoàcids. La distinció entre proteïnes i pèptids és arbitrària, però la convenció és que polipèptids per sota de 20-30 aminoàcids són considerats pèptids mentre que els més grans són considerats proteïnes.
Els pèptids naturals són presents al nostre organisme, on participen en múltiples processos. Els processos principals involucren la interaccióculdldlgjfjrjessos principals involucren la interaccire millor la seva funci amb macromolècules com les proteïnes. Per aquesta raó, els pèptids poden ser utilitzats com a agents terapèutics per tractar diferents malalties. Aquests potencials medicaments poden ser sintetitzats químicament mitjançant la síntesi de pèptids en fase sòlida (SPPS). Tot i que aquesta tècnica té múltiples avantatges, s’ha d’ajustar i dissenyar per a cada experiment per a que funcioni.
Tenint en compte que la majoria de dianes terapèutiques es troben dins les cèl·lules, els pèptids han de ser capaços de creuar les membranes cel·lulars, les quals actuen com a barreres. Certs tipus de pèptids, com els cíclics o bicíclics, han demostrat tenir l’habilitat de creuar membranes quan certs canvis es produeixen en la seva seqüència. En aquesta sessió pràctica, dissenyarem i sintetitzarem un pèptid terapèutic.
3. Disseny racional de medicaments
Antonija Kuzmanic (Orozco Lab)
Amb la determinació de l’estructura proteica mitjançant cristal·lografia de raig X, els científics poden utilitzar la informació obtinguda per trobar nous medicaments d’una forma innovadora. Combinant aquest enfoc amb mètodes computacionals emergents, el disseny racional no només ha abaratit els costos del disseny de fàrmacs, sinó que també ha fet possible el tractament de diverses malalties, inclòs a nivell personalitzat.
En aquest projecte, l’objectiuésaprendre com combinar la informació estructural amb mètodes computacionals, com l’ancoratge molecular, per descobrir nous fàrmacs. Cada estudiant tindrà un llistat de proteïnes que representen exemples satisfactoris de disseny racional de fàrmacs de la qual n’escolliran una. Estudiarem la base de l’estructura proteica, les característiques dels llocs d’unió, la selecció de lligants per aquests llocs d’unió i avaluarem quin dels compostos seleccionats podrien arribar a ser fàrmacs efectius mitjançant software d’ancoratge molecular.
4. Proteïnes de membrana. Quina pinta fan?
Arturo Rodríguez-Banqueri (Zorzano Lab)
S’estima que entre un 20-30% del proteosoma de molts organismes correspon a les proteïnes de membrana. Les proteïnes de membrana tenen una llarga llista de funcions, com per exemple el manteniment de l’homeòstasi cel·lular, la transmissió d’informació entre els espais intra i extra cel·lulars o entre compartiments intracel·lulars. No és sorprenent doncs que el mal funcionament de les proteïnes de membrana sigui causa directa d’importants patologies. De fet quasi el 50% dels fàrmacs actuals tenen com a diana proteïnes de membrana, jugant per tant un rol essencial en el descobriment i el desenvolupament de nous fàrmacs.
La cristal·lografia de rajos X, és actualment, una de les eines més potent que tenim per determinar l’estructura de les proteïnes a nivell atòmic. L’estructura d’aquestes proteïnes és utilitzada pel disseny de nous fàrmacs. Desafortunadament, obtenir cristalls d’alta qualitat de proteïnes de membrana per difracció de raigs Xésuna tasca difícil degut a la hidrofobicitat d’aquestes proteïnes. La baixa estabilitat en solució d’aquestes i la seva tendència a formar agregats són els grans problemes durant els estudis de cristal·lització.
En aquest curs veurem quines tècniques d’enginyeria de proteïnes s’utilitzen en l’actualitat per treballar amb proteïnes de membrana. En aquest pas, és essencial aconseguir una cristal·lització correcte per a obtenir una resolució apte per a obtenir l’estructura de la proteïna mitjançant cristal·lografia de raigs X.
5. Entenent l’ADN: Que et fa a tu diferent a la resta?
Aquest curs és una continuació del primer semestre
Joana Raquel Faria (Stracker Lab)
Es pot dir que l’ADN és el manual d’instruccions genètic de les nostres cèl·lules. Aquesta molècula conté la informació genètica que controla totes les funcions cel·lulars com la proliferació o l’apoptosi, o altres coses més complexes com el color dels nostres ulls. Tot i això, l’ADN pot patir alteracions que afectin aquests processos duent a processos patològics com el càncer. Per això les nostres cèl·lules han desenvolupat mecanismes de control per reparar tots els errors que puguin ocórrer al ADN, el que s’anomena via de resposta als danys a l’ADN. Es a dir, tenim certs gens, la funció dels quals és la de protegir el genoma, són responsables de mantenir l’estabilitat genòmica i protegir les nostres cèl·lules. Malgrat això, aquest sistema no actua igual per tothom i es per això que tot i tenir estils de vida similars algunes persones desenvolupin càncer i altres no.
En aquest curs, explorarem la relació entre la inestabilitat genòmica (canvia a l’ADN) i el càncer. Intentarem entendre els mecanismes pels quals el ADN controla les funcions cel·lulars i com les diferències genètiques que existeixen entre nosaltres influencien en el risc de patir càncer.
6. Cèl·lules mare, Modelització de malalties i descobriment de fàrmacs utilitzant...mosques?
Mahi Rahman (Casanova Lab)
Drosophila – Un meravellós insecte que ha sigut utilitzat per entendre biologia fonamental a nivell cel·lular i genètic durant més de cent anys. Amb una vida molt curta, només 4 cromosomes, sense isoformes en molts dels seus gents i molt anys de estudis científics han fet d’aquest invertebrat una eina eficient i molt útil per a l’estudi de moltes qüestions de la biologia actual. Aquests temes van des de les mutacions genètiques a efectes ambientals en la salut dels organismes. Amb el descobriment de les cèl·lules mare intestinals al 2006, Drosophila ha obert una nova frontera per explorar la biologia de les cèl·lules mare i la seva implicació en càncer, de fet, les cèl·lules mare són crucials per a la recaiguda del pacient.
A més de poder modelitzar el càncer, podem fer cribratges de fàrmacs sense el dispendi econòmic que suposa fer-ho en vertebrats.
En aquest curs, començarem amb una breu historia de Drosophila com a organisme model i quines són les seves avantatges i les seves limitacions. Estudiarem les cèl·lules mare intestinals i com podem modelar malalties com el càncer colorectal. Finalment, explicarem com podem fer un cribratge de compostos terapèutics utilitzant Drosophila. Durant aquest procés, aprendrem com dissenyar un projecte, treballar amb Drosophila, disseccionar i identificar diferents tipus cel·lulars, tècniques de microscòpia avançades com la microscòpia confocal. Aprendrem doncs, els avenços més innovadors en biomedicina.
Venue
CRAZY ABOUT BIOMEDICINE se realizará en las instalaciones de IRB Barcelona.
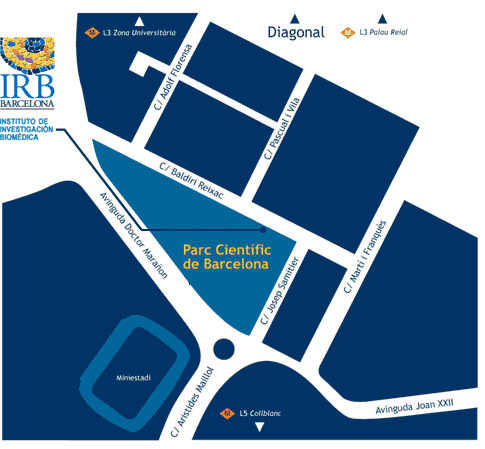
Lloc de celebració
IRB Barcelona
c/o Parc Cientific de Barcelona
Carrer Baldiri Reixac, 10
08028 Barcelona
(Campus de la Diagonal, Universitat de Barcelona)

