Images
- Un estudio del IRB Barcelona identifica que los genes de los ARN de transferencia (tRNA) acumulan mutaciones con una frecuencia hasta nueve veces superior.
- Estas mutaciones afectan especialmente a la zona que “lee” los codones y pueden dar lugar a tRNAs “quiméricos” que introducen errores sistemáticos en la fabricación de proteínas.
- El trabajo observa que estas mutaciones se acumulan con la edad, lo que abre una nueva vía para entender la pérdida de calidad de las proteínas y la fragilidad en la vejez.
La célula fabrica proteínas siguiendo instrucciones codificadas en el ARN mensajero, que se lee en grupos de tres letras llamados codones. Para traducir ese mensaje, utiliza unas moléculas llamadas ARN de transferencia (tRNA), que actúan como intermediarios: reconocen un codón concreto y aportan el aminoácido correspondiente para construir la proteína.
Un estudio de los laboratorios del Dr. Lluís Ribas de Pouplana y el Dr. Fran Supek, ambos en el IRB Barcelona, revela que los genes que producen tRNAs son puntos calientes de mutaciones (cambios en el ADN que se acumulan a lo largo de la vida en células del organismo) con la capacidad de alterar cómo se interpreta el código genético, y acelerar la pérdida funcional del proteoma. El trabajo se ha publicado hoy en Genome Research.
Un “punto ciego” del genoma: a más actividad, más mutación
La mayor parte de los estudios sobre mutaciones en cáncer se han centrado históricamente en genes que codifican proteínas. Sin embargo, el genoma humano contiene cientos de genes de tRNA, esenciales para asegurar la correcta traducción del mensaje genético a proteínas.
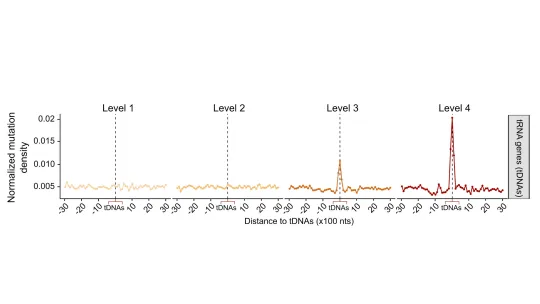
Al analizar datos de miles de genomas tumorales y muestras de tejido sano, el equipo observó que estos genes presentan tasas de mutación especialmente elevadas. Curiosamente, esta carga mutacional está directamente ligada a la actividad del gen: cuanto más se transcribe un tRNA (cuanto más "trabaja"), más probabilidades tiene de mutar. En algunos casos, la tasa de error es hasta nueve veces mayor que la de los genes convencionales.
Cuando el adaptador se equivoca: tRNAs “quiméricos”
Una parte crítica de cada tRNA es el anticodón, un triplete que reconoce los codones del ARN mensajero y determina qué aminoácido se incorpora a la proteína. El estudio describe que mutaciones en esta zona pueden generar tRNAs quiméricos: moléculas que siguen transportando un aminoácido, pero leen el codón de otro.
"Esto significa que la célula empieza a colocar de forma sistemática un aminoácido donde debería ir otro. Es como si en una fábrica de montaje, una pieza fuera sustituida repetidamente por otra incorrecta; al final, la estructura de las proteínas se vuelve inestable y esta inestabilidad del proteoma es una característica clave tanto del cáncer como del deterioro celular”, señala el Dr. Ribas de Pouplana.
Envejecimiento y pérdida de regeneración
Además de su impacto en la biología del cáncer, el trabajo indica que estas mutaciones se acumulan de forma lineal con la edad. Esto conecta con un problema fundamental del envejecimiento: la pérdida de proteostasis o capacidad de mantener las proteínas sanas.
“Este estudio abre una nueva dimensión para estudiar el envejecimiento. Contribuye a explicar por qué, con el paso de los años, perdemos la capacidad de fabricar y regenerar proteínas eficientemente, lo que se traduce en procesos de alto impacto sobre la calidad de vida de los ancianos, como la sarcopenia (pérdida de masa muscular) o la fragilidad general. Además, los errores en la traducción causados por tRNAs quiméricos inevitablemente resultarían en la precipitación de proteinas, un fenómeno directamente ligado a procesos de neurodegeneración como la enfermedad de Alzheimer", añade el Dr. Ribas de Pouplana.
Próximos pasos
El descubrimiento de estos "errores de traducción" programados genéticamente abre nuevas vías para explorar la biología del envejecimiento. El equipo investiga ahora si la generación de tRNAs quiméricos está acelerada, y si existen mecanismos celulares que intentan compensar este caos genético antes de que sea irreversible.
Artículo de referencia:
Age-dependent mutational loads in human tRNA genes are tumor-specific and result in chimeric tRNA sequences that could disrupt the genetic code
Marina Murillo, Marina Salvadores, Aina Vaquer Picó, Lina Tsapanou, Adrian Gabriel Torres, Fran Supek & Lluis Ribas de Pouplana
Genome Research (2026) 10.1101/gr.281022.125
IRB Barcelona
El Instituto de Investigación Biomédica (IRB Barcelona) trabaja para conseguir una vida libre de enfermedades. Desarrolla una investigación multidisciplinar de excelencia para curar el cáncer y otras enfermedades vinculadas al envejecimiento. Establece colaboraciones con la industria farmacéutica y los principales hospitales para hacer llegar los resultados de la investigación a la sociedad, a través de la transferencia de tecnología, y realiza diferentes iniciativas de divulgación científica para mantener un diálogo abierto con la ciudadanía. El IRB Barcelona es un centro internacional que acoge alrededor de 400 científicos de más de 30 nacionalidades. Reconocido como Centro de Excelencia Severo Ochoa desde 2011, es un centro CERCA y miembro del Barcelona Institute of Science and Technology (BIST).