Images
Esta misma molécula también está involucrada en cáncer y los estudios sobre su actividad pueden dar nuevas pistas para diseñar terapias eficaces.
Científicos del Instituto de Investigación Biomédica (IRB Barcelona), liderados por el Investigador ICREA Marco Milán, revelan una sorprendente nueva función de la proteína Notch, opuesta a la conocida hasta hoy. La proteína Notch está ubicada en las membranas de las células y activa una cascada de señales que regula la expresión de genes que harán que la célula se divida, crezca, migre, se especialice o muera. La actividad de Notch se requiere para el correcto desarrollo de los seres vivos y para el mantenimiento de los tejidos en adultos. Cuando actúa en el momento o contexto erróneo, Notch puede dar lugar a la generación de tumores, entre los que figuran leucemias, cáncer de mama, de colon, de piel, de pulmón, o carcinomas renales.
Milán: “Todo nuevo dato sobre la modulación de la actividad de Notch puede ser relevante para diseñar terapias eficaces contra el cáncer.”
“Las mismas vías que dirigen el desarrollo y el crecimiento de los seres vivos están implicadas en la transformación de células normales en cancerosas”, dice Marco Milán, así que “todo nuevo dato sobre la modulación de la actividad de Notch, el primer paso en la cadena, puede ser relevante para diseñar terapias eficaces”. El grupo de Marco Milán ha descubierto ahora que la presencia de la proteína Notch en la membrana de las células también es necesaria para inactivar la vía, además de para activarla. La descripción del nuevo rol de Notch y el mecanismo que lo regula, hallado en la mosca Drosophila melanogaster, es el tema de portada de la revista Current Biology, del grupo Cell.
¡Stop! Notch es un agente doble
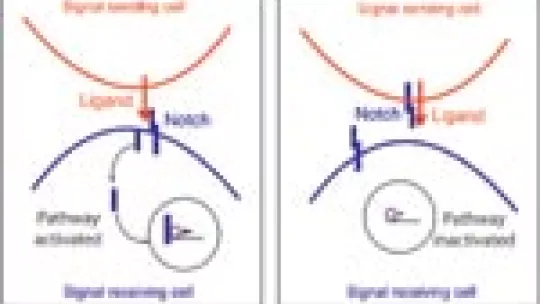
Para que la vía de Notch se active, proteínas de tipo ligando de células vecinas se unen al receptor. Al contactar ligando y receptor, el receptor Notch se procesa y la parte intracelular se va al núcleo para activar la expresión de genes. Éste es el sistema básico y “extremadamente simple” de activación de la vía de Notch, basado en el contacto de corto alcance entre células a través de un ligando y un receptor.
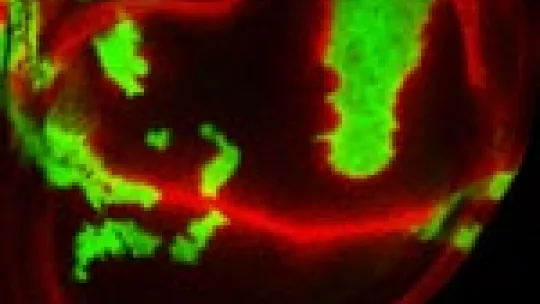
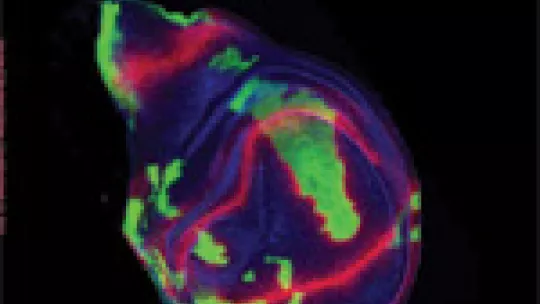
En un ala en desarrollo y mediante una técnica denominada Análisis Clonal, los investigadores manipularon grupos de células, entre células perfectamente normales, para que no expresaran el receptor Notch. Los científicos usan el ala de Drosophila porque es un excelente modelo para descubrir cómo se comportan las células cuando se les muta un gen determinado y comprobar cómo afecta a las células adyacentes. Este era el propósito del estudio diseñado por Isabelle Becam, investigadora postdoctoral del grupo de Milán y primera autora del artículo. “Como era de esperar, las células carentes de Notch no activaban la vía, pero lo sorprendente fue observar que las células vecinas sí lo hacían”. ¿Podía ser la ausencia de Notch en el grupo de células mutadas la causa de la activación?, se preguntó Becam.
Efectivamente, los análisis demostraron que es el mismo receptor Notch quien secuestra a los ligandos para evitar que se conecten a los receptores Notch de las células contiguas. Los experimentos demostraron que la ausencia del receptor en las células manipuladas deja muchos ligandos libres, listos para entrar en contacto con receptores Notch de las células sin manipular. “Es curioso, pero en la célula ‘emisora’ de la señal el receptor Notch captura a los ligandos actuando de silenciador, mientras que en la célula ‘receptora’ de señal la unión de los ligandos con Notch permite la activación de la vía”. “En realidad”, dice Milán, “se trata de un delicado equilibrio entre ligandos y receptores de las células emisoras y receptoras”. En otras palabras, Notch es una especie de agente doble y tiene funciones opuestas: reprime o activa la vía según se localiza en células emisoras o receptoras de señal. Es de resaltar la existencia de múltiples mecanismos de represión para un sistema de activación tan sencillo, “precisamente por ser una vía de señalización muy importante, pero a su vez peligrosa”, explica Milán.
Milán: “Nuestro estudio sugiere que no sería un buena estrategia bloquear el receptor Notch para combatir las leucemias T-ALL.”
Los investigadores han encontrado este mecanismo de auto-represión de Notch en Drosophila y ahora debería comprobarse si también funciona en ratón y humanos. Lo más probable es que sí, ya que el sistema ligando-receptor de activación de Notch se ha conservado en todos los organismos. “Si este nuevo mecanismo también funciona en vertebrados, debería tenerse en consideración de cara a diseñar terapias efectivas contra determinados tipos de cáncer, como las T-ALL o leucemias linfoblásticas agudas T”, concluye Milán.
Está bien establecido que la vía de Notch controla el desarrollo de los linfocitos T, un tipo de células inmunitarias de la sangre. Las células que deben madurar para desarrollarse en linfocitos reciben las señales adecuadas a través de los receptores Notch. Más de la mitad de los pacientes con T-ALL tienen el receptor Notch permanentemente activo en las células precursoras de linfocitos T, lo cual estimula la continua proliferación de células hasta formar tumores. “A priori, bloquear el receptor Notch podría parecer una buena estrategia para combatir este tipo de leucemias. No obstante, los resultados de nuestro trabajo sugieren que no, porque bloqueando el receptor sólo en algunas células provocaría efectos indeseados en células adyacentes”, advierte Milán.
Artículo de referencia
A role of Notch in ligand cis-inhibition in Drosophila.
Isabelle Becam, Ulla-Maj Fiuzza, Alfonso Martínez-Arias and Marco Milán.
Current Biology, 2009. doi: 10.1016/j.cub.2010.01.058
IRB Barcelona
El Instituto de Investigación Biomédica (IRB Barcelona) trabaja para conseguir una vida libre de enfermedades. Desarrolla una investigación multidisciplinar de excelencia para curar el cáncer y otras enfermedades vinculadas al envejecimiento. Establece colaboraciones con la industria farmacéutica y los principales hospitales para hacer llegar los resultados de la investigación a la sociedad, a través de la transferencia de tecnología, y realiza diferentes iniciativas de divulgación científica para mantener un diálogo abierto con la ciudadanía. El IRB Barcelona es un centro internacional que acoge alrededor de 400 científicos de más de 30 nacionalidades. Reconocido como Centro de Excelencia Severo Ochoa desde 2011, es un centro CERCA y miembro del Barcelona Institute of Science and Technology (BIST).