Images
Investigadors de l’IRB Barcelona localitzen una peça decisiva de la maquinària que permet a l’Staphylococcus aureus transferir-se gens de resistència a antibiòtics.
Els bacteris S. aureus representen una amenaça letal en hospitals d’arreu del món.
Interrompre la propagació de soques de bacteris resistents és una de les estratègies per combatre les infeccions als hospitals.
El bacteri Staphylococcus aureus mata 11.300 persones cada any només als Estats Units per infeccions resistents als antibiòtics, que corresponen a més de la meitat de les morts provocades per infeccions de bacteris resistents gram-positiu en aquell país. L’alta letalitat li atorga la rapidesa que tenen els bacteris en adquirir gens de resistència a antibiòtics. Un estudi de l’Institut de Recerca Biomèdica (IRB Barcelona), que ha comptat amb la col·laboració del Centro de Investigaciones Biológicas (CIB-CSIC) de Madrid, identifica la peça clau de la maquinària que usen els bacteris Staphylococcus aureus per adquirir i transferir-se gens que els fan resistents als antibiòtics. El treball s’ha publicat aquesta setmana a Proceedings of the National Academic of Sciences (PNAS).
“La lluita contra els bacteris, sobretot en entorns hospitalaris on són un problema de primera magnitud, passa per entendre com es transfereixen els gens per adaptar-se ràpidament a entorns canviants, com per exemple quan es troben amb antibiòtics nous”, assenyala el líder de l’estudi i científic de l’IRB Barcelona Miquel Coll, també investigador del CSIC, que estudia la transferència horitzontal de gens des de la biologia estructural.
Impedir la propagació
“Una habilitat extraordinària dels bacteris per evolucionar i adaptar-se ràpidament és aquesta transferència horitzontal de gens, que els humans per exemple no tenim”, explica Coll. Una d’aquestes vies s’anomena conjugació: dos bacteris s’uneixen per passar-se un tros d’ADN, anomenat plàsmid. “Un plàsmid és un tros petit d’ADN en forma de cercle que conté molt pocs gens, on es localitzen normalment gens selectius de resistència a antibiòtics, i que triguen només uns minuts a ser transferits entre bacteris”, detalla.
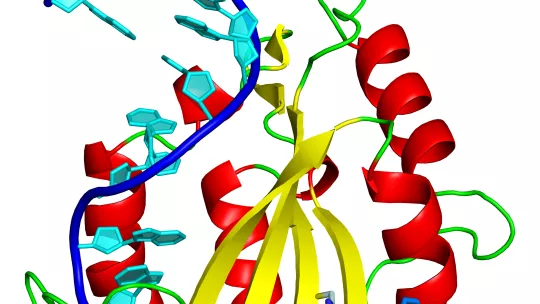
En la transferència horitzontal intervé una maquinària a on la relaxasa, una proteïna enzimàtica, és una peça clau. Gràcies a la resolució de l’estructura en tres dimensions del complex que forma la relaxasa amb l’ADN del plàsmid, els investigadors han identificat un aminoàcid, una histidina, com l’element central perquè es produeixi la transferència i es propagui la resistència.
“El que és nou és que la relaxasa de diferents soques de Staphylococcus aureus és especial perquè usa un aminoàcid que no s’havia vist mai en cap altre de les relaxases que coneixem”, precisa el primer signant de l’estudi, Radoslaw Pluta, estudiant de doctorat de “la Caixa” a l’IRB Barcelona, i actualment investigador postdoctoral al International Institute of Molecular and Cell Biology a Varsòvia, Polònia.
La histidina és el residu catalític, que permet a la relaxasa tallar l’ADN, unir-s’hi, estirar una de les dues cadenes i endur-se-la per traspassar-la al bacteri receptor, on la cadena es replicarà per formar de nou la doble cadena del plàsmid. Aquest nou plàsmid ja contindrà els gens de resistència i la maquinària per transferir-los a un altre bacteri. Els científics informen que aquesta histidina catalítica està present en les relaxases del 85% de soques del Staphylococcus aureus.
Per comprovar que la histidina és decisiva, els investigadors del grup de Manuel Espinosa del CIB-CSIC, que han participat en l’estudi, la van intercanviar per un aminoàcid diferent i van confirmar en plaques amb cultius que s’impedia la transferència.
La mutació de la histidina no mata el bacteri només impedeix la transferència de gens. Com es podria usar això per combatre les infeccions? “No ho sé”, admet Coll, “però ara sabem més detalls d’un bacteri letal i per tant ens podria conduir a desenvolupar molècules per evitar la propagació de soques resistents”.
Coll explica que les infeccions hospitalàries són les més difícils de combatre. “Ara mateix estem com en una carrera que sempre perdem perquè quan es treu un antibiòtic diferent de seguida apareixen resistències i es propaguen”, descriu. El científic afegeix que l’arsenal d’antibiòtics en reserva dels hospitals per tractar les infeccions resistents és “massa” curt. A banda de la dificultat de generar nous antibiòtics, Coll també ressalta com a escull per avançar més ràpidament el fet que “hi hagi poca inversió, ja que la indústria mostra altres prioritats. Això és legítim, per això cal fer inversions que sumin fons públics i privats”.
En aquest treball hi ha col·laborat el grup de Modesto Orozco, també a l’IRB Barcelona, que ha proporcionat l’estudi teòric que atorga validesa a la reacció química entre l’ADN del plàsmid i la proteïna a través de la histidina. La resolució de l’estructura del complex format per la proteïna i la cadena d’ADN s’ha realitzat amb dades obtingudes per difracció de raigs X al sincrotró europeu de Grenoble.
Article de referència:
Radoslaw Pluta, D. Roeland Boer, Fabián Lorenzo-Díaz, Silvia Russi, Hansel Gómez, Cris Fernández-López, Rosa Pérez-Luque, Modesto Orozco, Manuel Espinosa and Miquel Coll
PNAS (2017): doi: 10.1073/pnas.1702971114
Sobre l’IRB Barcelona
Creat el 2005 per la Generalitat de Catalunya i la Universitat de Barcelona, l'IRB Barcelona és Centre d'Excel·lència Severo Ochoa des de 2011. L’objectiu de l’IRB Barcelona és fer recerca d'excel·lència en biomedicina i millorar la qualitat de vida de les persones i, en paral·lel, potenciar la formació de talent, la transferència tecnològica i la comunicació social de la ciència. Els 25 laboratoris i set plataformes tecnològiques treballen per respondre a preguntes bàsiques en biologia i orientades a malalties com ara el càncer, la metàstasi, l’Alzheimer, la diabetis i malalties rares. És un centre internacional que acull al voltants de 400 treballadors de 32 nacionalitats. Està ubicat en el Parc Científic de Barcelona. L’IRB Barcelona forma part del Barcelona Institute of Science and Technology (BIST) i la xarxa de Centres de Recerca de Catalunya (CERCA).
IRB Barcelona
L’Institut de Recerca Biomèdica (IRB Barcelona) treballa per aconseguir una vida lliure de malalties. Desenvolupa una recerca multidisciplinària d’excel·lència per curar el càncer i altres malalties vinculades a l'envelliment. Treballa establint col·laboracions amb la indústria farmacèutica i els principals hospitals per fer arribar els resultats de la recerca a la societat a través de la transferència de tecnologia, i du a terme diferents iniciatives de divulgació científica per mantenir un diàleg obert amb la ciutadania. L’IRB Barcelona és un centre internacional que acull al voltant de 400 investigadors de més de 30 nacionalitats. Reconegut com a Centre d'Excel·lència Severo Ochoa des de 2011, és un centre CERCA i membre del Barcelona Institute of Science and Technology (BIST).