Images
A l’estudi, publicat a Cell Reports, s’ha inhibit la capacitat de RAS de bloquejar la mort cel·lular, aconseguint així eliminar tumors malignes sense afectar el desenvolupament dels òrgans.
Els resultats de l’estudi obren la possibilitat d’utilitzar teràpies combinades d’irradiació i d’administració d’inhibidors de la via de RAS per eliminar cèl·lules tumorals.
L’oncogèn RAS està activat en el 30% dels càncers humans, donant lloc a la proliferació i transformació de les cèl·lules tumorals. Fins el moment, no s’havia trobat cap inhibidor efectiu per a aquesta proteïna.
Marco Milán, cap del Laboratori de Desenvolupament i Control del Creixement de l’Institut de Recerca Biomèdica (IRB Barcelona),ha liderat un estudi publicat a Cell Reports mitjançant el qual s’ha identifica el punt feble de les cèl·lules on l'oncogèn RAS està actiu.
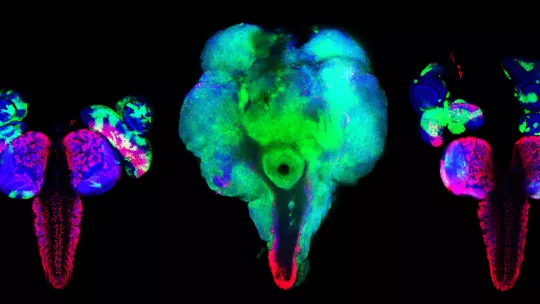
El laboratori de Milán ha utilitzat la mosca del vinagre, Drosophila melanogaster, com a model per demostrar que els nivells alts de proliferació cel·lular induïts per RAS poden ser explotats terapèuticament amb l'objectiu de definir estratègies per eliminar específicament cèl·lules tumorals que expressin aquest oncogèn.
Tal i com explica Milán, investigador ICREA de l’IRB Barcelona: “Les cèl·lules RAS dupliquen el seu ADN molt ràpidament, per la qual cosa generen errors i danys a l’ADN. Hem demostrat que RAS bloqueja la reparació d’aquests danys. En cèl·lules normals, això generaria la mort cel·lular per l’activació de la proteïna supressora de tumors p53. No obstant, RAS bloqueja la capacitat de matar aquesta proteïna, i aquest és exactament el punt que hem explotat tant amb teràpia genètica com química”.
En l'estudi s'ha inhibit la capacitat de RAS de bloquejar la mort cel·lular, aconseguint d'aquesta forma eliminar, selectivament i per mort cel·lular, tumors malignes sense afectar el desenvolupament dels òrgans i de l'animal.Per a això, s'ha utilitzat TRAMETINIB, un fàrmac que es recepta per al melanoma humà.
En paraules de Lada Murcia i Marta Clemente, primeres autores d’aquest treball, “també hem demostrat que la radioteràpia, una font externa de dany a l’ADN, incrementa la sensibilitat de cèl·lules que expressen RAS a teràpia genètica”. “Els resultats de l’estudi”, conclou Milán, “obren la possibilitat d’utilitzar teràpies combinades d’irradiació i d’administració d’inhibidors de la via de RAS per eliminar selectivament cèl·lules tumorals”.
L’estudi ha rebut finançament del Ministeri de Ciència, Innovació i Universitats, i s’ha dut a terme amb la col·laboració d’Anne Royou, en l’Institut Européen de Chimie et Biologie, a Bordeus (França).
Article de referència:
Lada Murcia, Marta Clemente-Ruiz, Priscillia Pierre-Elies, Anne Royou, and Marco Milán
Selective killing of RAS-malignant tissues by exploiting oncogene-induced DNA damage
Cell Reports(2019) DOI: 10.1016/j.celrep.2019.06.004
IRB Barcelona
L’Institut de Recerca Biomèdica (IRB Barcelona) treballa per aconseguir una vida lliure de malalties. Desenvolupa una recerca multidisciplinària d’excel·lència per curar el càncer i altres malalties vinculades a l'envelliment. Treballa establint col·laboracions amb la indústria farmacèutica i els principals hospitals per fer arribar els resultats de la recerca a la societat a través de la transferència de tecnologia, i du a terme diferents iniciatives de divulgació científica per mantenir un diàleg obert amb la ciutadania. L’IRB Barcelona és un centre internacional que acull al voltant de 400 investigadors de més de 30 nacionalitats. Reconegut com a Centre d'Excel·lència Severo Ochoa des de 2011, és un centre CERCA i membre del Barcelona Institute of Science and Technology (BIST).