Images
- Un grupo de investigadores, liderados por Maria Macias, investigadora ICREA del IRB Barcelona, detalla el mecanismo que usa el factor TGIF1 para inhibir la función de las proteínas Smads.
- El trabajo, que ha utilizado técnicas de biología molecular y estructural para estudiar esta interacción se ha publicado en Nucleic Acids Research
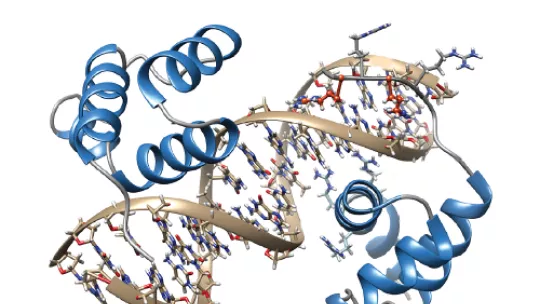
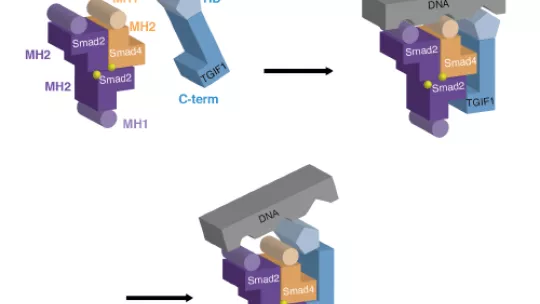
Conocer el mecanismo de interacción entre las proteínas Smad, involucradas en muchos aspectos del desarrollo celular, y su principal inhibidor, la proteína TGIF1, abre la vía al diseño de moléculas específicas para tratar un amplio espectro de condiciones/alteraciones médicas. El laboratorio de Caracterización estructural de los complejos macromoleculares del Instituto de Investigación Biomédica (IRB Barcelona), ha detallado este mecanismo de interacción y ha confirmado que TGIF1 inhibe las proteínas Smad, ocupando la región que se une al ADN. Si las proteínas Smad no pueden unirse al ADN no son capaces de realizar su función como factores de transcripción y se bloquea así la cascada de señalización de TGF-beta.
Una vía de señalización casi universal
Las vías de señalización están formadas por un grupo de biomoléculas que trabajan juntas para controlar una o más funciones de las células. En una vía de señalización una molécula activa y/o interacciona con otras, estas a su vez activan a otras y así sucesivamente en lo que se conoce como un efecto cascada.
Las proteínas Smad forman parte de la vía de señalización orquestada por la familia de hormonas TGF-β, y está conservada en todos los animales multicelulares. Los Smads forman una familia de factores de transcripción que activan e inhiben la transcripción de genes influyendo en aspectos clave como el desarrollo embrionario, la regeneración de tejidos y la respuesta inmunitaria. La proteína TGIF1 es uno de los principales factores conocidos hasta ahora que inhibe a las proteínas Smad y, en caso de mutación, se relaciona con la holoprosencefalia (una malformación congénita grave del cerebro y la cara) así como con la progresión de tumores en varios tipos de cánceres.
"Creemos que nuestro estudio será de gran interés para muchos grupos en todo el mundo que están estudiando el impacto de la señalización TGF beta en el cáncer y otras enfermedades", apunta Maria Macias.
Una interacción sinérgica
La interacción entre las Smad y la TGIF1 se había predicho en numerosos trabajos anteriores mediante experimentos bioquímicos y celulares. El equipo de investigadores liderado por Macias, ha utilizado técnicas de biología molecular y estructural como los rayos-X y la resonancia magnética nuclear (NMR) para conocer en detalle la interacción.
Este estudio ha confirmado que las Smads tienen múltiples sitios de interacción, que pueden actuar sinérgicamente, aumentando así la complementariedad y la especificidad de las uniones. Otra conclusión destacada es que las regiones que previamente se consideraba que tenían la función de unirse exclusivamente al ADN, se ha visto que también participan en interacciones con otras proteínas y cofactores, “La identificación de los sitios de unión de Smad para los cofactores revelaría la presencia de nuevas regiones diana que podrían usarse como objetivos terapéuticos”, explica Maria Macias.
El proyecto ha contado con la participación de la Unidad de investigación en síntesis asimétrica y se ha financiado con fondos competitivos del Ministerio de Economía y Competitividad (ahora Ministerio de Ciencia, Innovación y Universidades), fondos BiomMedTec de la obra social ‘la Caixa’, la Fundación BBVA, CERCA, con una beca predoctoral ‘la Caixa’ y posdoctoral Marie Sklodowska-Curie COFUND y con fondos ICREA.
Artículo de referencia:
Ewelina Guca, David Suñol, Lidia Ruiz, Agnieszka Konkol, Jorge Cordero, Carles Torner, Eric Aragon, Pau Martin-Malpartida, Antoni Riera and Maria J. Macias
TGIF1 homeodomain interacts with Smad MH1 domain and represses TGF- β signaling
Nucleic Acids Research (2018) DOI: 10.1093/nar/gky680
IRB Barcelona
El Instituto de Investigación Biomédica (IRB Barcelona) trabaja para conseguir una vida libre de enfermedades. Desarrolla una investigación multidisciplinar de excelencia para curar el cáncer y otras enfermedades vinculadas al envejecimiento. Establece colaboraciones con la industria farmacéutica y los principales hospitales para hacer llegar los resultados de la investigación a la sociedad, a través de la transferencia de tecnología, y realiza diferentes iniciativas de divulgación científica para mantener un diálogo abierto con la ciudadanía. El IRB Barcelona es un centro internacional que acoge alrededor de 400 científicos de más de 30 nacionalidades. Reconocido como Centro de Excelencia Severo Ochoa desde 2011, es un centro CERCA y miembro del Barcelona Institute of Science and Technology (BIST).