Images
La enfermedad de Kennedy es un trastorno neuromuscular sin tratamiento considerado una enfermedad rara
Un estudio dirigido por Xavier Salvatella puede abrir el camino a nuevas líneas de tratamiento de la enfermedad de Kennedy
La enfermedad de Kennedy es una enfermedad neuromuscular rara causada por una mutación de la proteína receptora de andrógenos. El Laboratorio de Biofísica Molecular dirigido por Xavier Salvatella en el Instituto de Investigación Biomédica (IRB Barcelona) ha hallado recientemente nuevas características estructurales claves del receptor androgénico inducidas por la mutación. Estas conclusiones se han publicado en la revista Nature Communications y podrían abrir nuevas vías terapéuticas para una familia de enfermedades raras incurables denominadas enfermedades de expansión de poliglutamina (polyQ).
La atrofia muscular espinal y bulbar (AMEB), también conocida como enfermedad de Kennedy, es un trastorno neuromuscular sin tratamiento que merma de forma drástica la calidad de vida de los pacientes. Está clasificada como enfermedad rara, de modo que afecta a menos de 5 de cada 10.000 personas. La mutación de la proteína receptora de andrógenos que causa la enfermedad es una expansión de una secuencia repetitiva de aminoácidos que contiene únicamente residuos de glutamina, denominada tracto polyQ. Curiosamente, la longitud de este tracto determina si una persona desarrolla la enfermedad de Kennedy.
También se puede hallar una mutación similar en otras enfermedades de expansión de polyQ, siendo la más conocida de ellas la enfermedad de Huntington. Se desconocen los motivos por los cuales una expansión del tracto polyQ conduce al desarrollo de enfermedades de expansión de polyQ. En el caso de la enfermedad de Kennedy, los investigadores creen que las proteínas receptoras de andrógenos que contienen una poliglutamina muy larga tienden a oligomerizar. Estos oligómeros generan entonces agregados de proteínas tóxicas en el interior de la célula, lo que impide su buen funcionamiento.
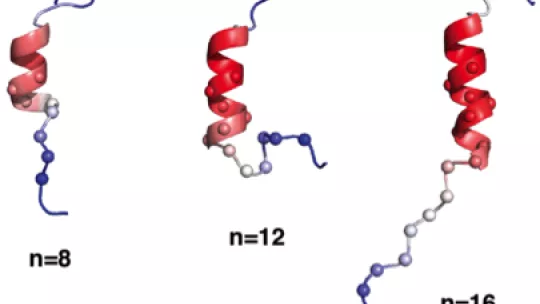
Para que una proteína funcione correctamente, debe plegarse en una estructura tridimensional ordenada. Hasta el momento, se creía que la parte de la proteína receptora de andrógenos que contenía la expansión de polyQ era desordenada y, por lo tanto, no se podía plegar en esta estructura. En 2016, el grupo de Salvatella descubrió que el tracto polyQ del receptor androgénico podía adoptar una estructura helicoidal. “Fue un hallazgo muy interesante, puesto que hasta ahora se creía que estos tractos no adoptan ninguna estructura específica”, explica Salvatella.
En el estudio actual, el equipo dio un paso más y visualizó la hélice de la proteína del tracto polyQ a través de métodos biofísicos y computacionales avanzados. Ahora informan que esta región específica puede formar hélices muy ordenadas y, fundamentalmente, que la expansión de polyQ aumenta considerablemente el grado de orden y estabilidad de estas hélices. Esta información amplía nuestra comprensión de la función de los receptores androgénicos.
Albert Escobedo, investigador posdoctoral del IRB Barcelona y primer coautor del estudio, explica: “Nuestras conclusiones indican que los tractos polyQ largos mutados pueden formar hélices cada vez más estables. Esto sugiere que pueden causar trastornos de poliglutamina como la enfermedad de Kennedy”. Destaca que “atacar esas hélices con fármacos puede ser una vía terapéutica para estos trastornos actualmente incurables.”
Este estudio fue financiado con subvenciones de La Marató de TV3, el Consejo Europeo de Investigación (ERC) y el Ministerio de Ciencia, Innovación y Universidades (anteriormente conocido como MINECO).
Articulo de referencia:
Albert Escobedo, Busra Topal, Micha B. A. Kunze, Juan Aranda, Giulio Chiesa, Daniele Mungianu, Ganeko Bernardo-Seisdedos, Bahareh Eftekharzadeh, Margarida Gairí, Roberta Pierattelli, Isabella C. Felli, Tammo Diercks, Oscar Millet, Jesús García, Modesto Orozco, Ramon Crehuet, Kresten Lindorff-Larsen and Xavier Salvatella.
Side chain to main chain hydrogen bonds stabilize a polyglutamine helix in a transcription factor.
Nature Communications (2019) DOI: 10.1038/s41467-019-09923-2
IRB Barcelona
El Instituto de Investigación Biomédica (IRB Barcelona) trabaja para conseguir una vida libre de enfermedades. Desarrolla una investigación multidisciplinar de excelencia para curar el cáncer y otras enfermedades vinculadas al envejecimiento. Establece colaboraciones con la industria farmacéutica y los principales hospitales para hacer llegar los resultados de la investigación a la sociedad, a través de la transferencia de tecnología, y realiza diferentes iniciativas de divulgación científica para mantener un diálogo abierto con la ciudadanía. El IRB Barcelona es un centro internacional que acoge alrededor de 400 científicos de más de 30 nacionalidades. Reconocido como Centro de Excelencia Severo Ochoa desde 2011, es un centro CERCA y miembro del Barcelona Institute of Science and Technology (BIST).