Images
Nature Medicine publica un treball pioner sobre una proteïna que regula l'expressió de centenars de gens amb un paper fonamental en la progressió del càncer de pàncrees, gliomes i, possiblement, en molts altres tipus de tumors.
Un treball dirigit pels investigadors Raúl Méndez, professor ICREA de l'Institut de Recerca Biomèdica (IRB Barcelona) i Pilar Navarro de l'IMIM (Institut de Recerca Hospital del Mar, Barcelona), descriu un nou mecanisme de reprogramació de l'expressió de gens que transformen una cèl·lula sana en tumoral. En l'estudi, que es publica a Nature Medicine aquesta setmana, els investigadors han identificat la proteïna CPEB4 com un director d'orquestra cel·lular que "encén" centenars de gens vinculats al creixement tumoral.
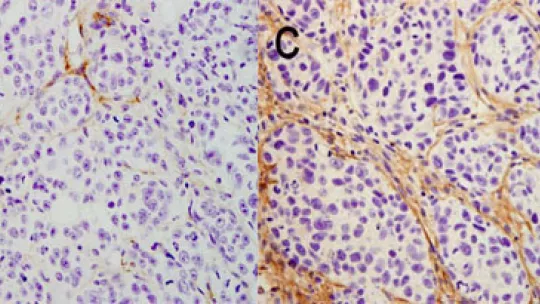
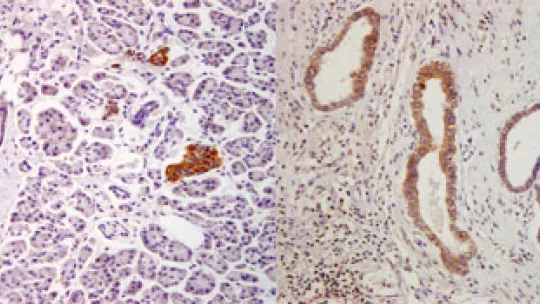
"La novetat radica en què no seria només la mutació d'un gen concret el que promouria el creixement del tumor, sinó l'expressió en el lloc incorrecte d'una proteïna que "activa" centenars de molècules missatgeres (mARNs) que porten la informació continguda en els gens per sintetitzar les proteïnes, sense que aquests gens estiguin mutats. Això origina l'expressió de multitud de gens "normals" però en quantitats i en moments anormals, més propis de les etapes primerenques de desenvolupament de l'embrió que d'òrgans adults", explica Raúl Méndez, expert en la família de proteïnes CPEB, que va iniciar el treball al CRG per continuar-lo a l’IRB Barcelona. "Aquest seria el cas del tPA (activador tissular del plasminògen), una proteïna que normalment no es troba en el pàncrees sa i que, no obstant això, presenta nivells molt alts en tumors de pàncrees", matisen Elena Ortiz-Zapater, primera autora de l’article, i Pilar Navarro.
Sense CEPB4 els tumors es redueixen en un 80%
Una conclusió destacada del treball és que en els teixits estudiats, pàncrees i cervell, CPEB4 no es detecta en cèl·lules normals sinó només en les tumorals, pel que la seva inhibició seria un tractament antitumoral molt específic i amb molt pocs efectes adversos, "una de les principals limitacions avui de moltes de les teràpies antitumorals", diu Pilar Navarro, científica especialista en càncer de pàncrees. De fet, aquest treball mostra, mitjançant estudis realitzats en ratolí amb cèl·lules de tumors de pacients, que la disminució dels nivells de CPEB4 en les cèl·lules canceroses, redueix la mida dels tumors fins a un 80%.
Encara que de moment l'estudi es limita a dos tipus de tumors, segons els científics coautors, "tenint en compte els efectes observats en els tumors estudiats i el tipus de gens regulats per aquest mecanisme, és d'esperar que participi en molts altres tumors". Aquest treball obre una nova via per dissenyar nous tractaments contra el càncer, pel que els investigadors estan dissenyant i analitzant inhibidors de CPEB4 amb possible valor terapèutic. "Les aplicacions a nivell clínic són molt prometedores encara que es necessita molt treball de recerca per identificar molècules inhibidores i testades en diferents models abans de determinar el seu potencial clínic i, si s'escau, que puguin ser utilitzades en pacients", adverteixen Navarro i Méndez.
En l'estudi han participat Francisco X. Real del Centro Nacional de Investigaciones Oncológicas (CNIO) i Eduardo Eyras, investigador ICREA, ambdós del Departament de Ciències Experimentals i de la Salut de la Universitat Pompeu Fabra; junt a Mar Iglesias y Francesc Alameda, del Servei de Patologia de l’Hospital del Mar.
Article de referència:
Key contribution of CPEB4-mediated translational control to cancer progression.
Elena Ortiz-Zapater, David Pineda, Neus Martínez-Bosch, Gonzalo Fernández-Miranda, Mar Iglesias, Francesc Alameda, Mireia Moreno, Carolina Eliscovic, Eduardo Eyras, Francisco X. Real, Raúl Méndez and Pilar Navarro.
Nature Medicine (2011) doi: 10.1038/nm.2540
IRB Barcelona
L’Institut de Recerca Biomèdica (IRB Barcelona) treballa per aconseguir una vida lliure de malalties. Desenvolupa una recerca multidisciplinària d’excel·lència per curar el càncer i altres malalties vinculades a l'envelliment. Treballa establint col·laboracions amb la indústria farmacèutica i els principals hospitals per fer arribar els resultats de la recerca a la societat a través de la transferència de tecnologia, i du a terme diferents iniciatives de divulgació científica per mantenir un diàleg obert amb la ciutadania. L’IRB Barcelona és un centre internacional que acull al voltant de 400 investigadors de més de 30 nacionalitats. Reconegut com a Centre d'Excel·lència Severo Ochoa des de 2011, és un centre CERCA i membre del Barcelona Institute of Science and Technology (BIST).