Images
El laboratori de Càncer Colorectal de l'IRB Barcelona identifica la síntesi de proteïnes (o capacitat biosintètica) com a propietat clau per a la potencialitat regeneradora de les cèl·lules de càncer de còlon.
El treball, publicat a Cell Stem Cell, proposa un nou enfocament terapèutic que la comunitat científica i les farmacèutiques hauran d'explorar.
Els tumors no són una massa uniforme de cèl·lules. En el càncer de còlon trobem cèl·lules diferenciades, semblants a les cèl·lules funcionals pròpies de la paret intestinal, i cèl·lules pluripotents, les cèl·lules mare del tumor. Aquestes cèl·lules mantenen el creixement tumoral i són les causants de les metàstasis. Un grup d'investigadors liderat per Eduard Batlle, investigador ICREA, cap de grup al CIBER de Càncer (CIBERONC), i cap del laboratori de Càncer Colorectal de l'IRB Barcelona, ha demostrat que l'essència de la pluripotencialitat resideix en la capacitat de sintetitzar proteïnes, una propietat que es podria utilitzar com a diana terapèutica.
"Les teràpies actuals contra el càncer de còlon no són eficaces perquè no aconsegueixen eliminar totes les cèl·lules pluripotents. Diversos grups de recerca, inclòs el nostre, hem observat que fins i tot quan s'eliminen les cèl·lules mare del càncer mitjançant estratègies experimentals, algunes cèl·lules diferenciades poden tornar a l'estat original pluripotent i regenerar el tumor. És un fenomen què anomenem plasticitat cel·lular", explica Batlle.
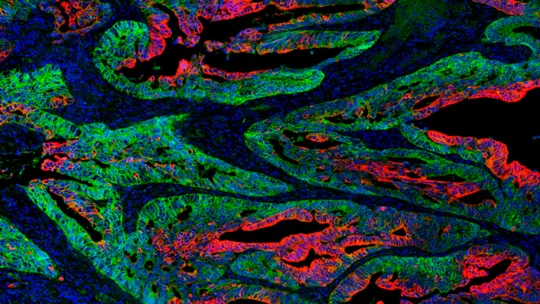
En aquest treball, el grup de Càncer Colorectal de l'IRB Barcelona ha observat que la síntesi de proteïnes en els tumors, té lloc en regions concretes, que coincideixen amb els nínxols de les cèl·lules mare del tumor. De fet, els tumors mostren un gradient de producció de proteïnes i, un cop aquesta activitat s'esgota, les cèl·lules perden de manera irreversible la capacitat de tornar a l'estat de cèl·lula mare del càncer. Per tant, és la capacitat biosintètica la que permet a les cèl·lules mare del tumor contribuir de manera il·limitada al creixement tumoral.
"Aquest descobriment va dirigit a intentar erradicar les cèl·lules mare del càncer basant-nos en el que fan, i no tant en el que són" explica Batlle. "A partir d’aquestes dades, la comunitat científica i farmacèutica es podrà plantejar si és possible dissenyar i assajar maneres d'interferir terapèuticament amb la capacitat biosintètica en les cèl·lules mare tumorals per frenar el creixement dels tumors i prevenir les metàstasis", afegeix.
Bloquejar la capacitat biosintètica atura el creixement del tumor
"Utilitzant models de càncer de còlon en ratolins, observem que bloquejant la capacitat de produir proteïnes o eliminant les cèl·lules tumorals amb aquesta propietat, vam aconseguir frenar el creixement del tumor de forma irreversible. Ara el següent pas és estudiar els senyals de l'entorn tumoral que confereixen o mantenen la capacitat biosintètica a certes cèl·lules del tumor", explica Clara Morral, una de les primeres autores de l'estudi. L'altra primera autora és Jelena Stanisavljevic, alumni de l'IRB Barcelona i, actualment, investigadora postdoctoral a l'Institut de Ciències Fotòniques (ICFO).
Organoids i CRISPR, claus per una recerca exitosa
El treball s'ha dut a terme utilitzant organoids, mini-tumors derivats de pacients i cultivables al laboratori, que permeten estudiar l'heterogeneïtat i organització cel·lular dels tumors. El sistema d’organoids, és una eina important per recrear els tumors dels pacients i estudiar millor la biologia del càncer i la seva interacció amb els teixits. L'estudi també ha requerit la modificació genètica de les cèl·lules tumorals mitjançant la tècnica de CRISPR-CAS9. Aquesta tècnica ha permès eliminar específicament les cèl·lules amb capacitat biosintètica per avaluar la seva contribució al creixement del tumor.
L'estudi s'ha realitzat amb la col·laboració dels grups de Scott Lowe, del Memorial Sloan Kettering Cancer Center, Lukas Dow del Weill-Cornell Medical College a New York, Alberto Villanueva de l'IDIBELL i Holger Heyn del CNAG-CRG. Aquest treball ha estat possible gràcies al finançament d'ERC Advanced Grant, Worlwide Cancer Research Grant i AGAUR; i les beques de la beques a investigadors del programes de La Caixa, Miguel Servet, Juan de la Cierva i AECC.
Reference article:
Clara Morral, Jelena Stanisavljevic, XavierHernando-Momblona, Elisabetta Mereu, Adrián Álvarez-Varela, CarmeCortina, Diana Stork, Felipe Slebe, Gemma Turon, Gavin Whissell, Marta Sevillano, Anna Merlos-Suárez, Àngela Casanova-Martí, Catia Moutinho, Scott W. Lowe, Lukas E. Dow, Alberto Villanueva, Elena Sancho, Holger Heyn, & Eduard Batlle
Zonation of Ribosomal DNA Transcription Defines a Stem Cell Hierarchy in Colorectal Cancer
Cell Stem Cell (2020) doi: 10.1016/j.stem.2020.04.012
Coneix el nostre Repte Metàstasi per sumar tota la societat en la recerca contra la metàstasi.
IRB Barcelona
L’Institut de Recerca Biomèdica (IRB Barcelona) treballa per aconseguir una vida lliure de malalties. Desenvolupa una recerca multidisciplinària d’excel·lència per curar el càncer i altres malalties vinculades a l'envelliment. Treballa establint col·laboracions amb la indústria farmacèutica i els principals hospitals per fer arribar els resultats de la recerca a la societat a través de la transferència de tecnologia, i du a terme diferents iniciatives de divulgació científica per mantenir un diàleg obert amb la ciutadania. L’IRB Barcelona és un centre internacional que acull al voltant de 400 investigadors de més de 30 nacionalitats. Reconegut com a Centre d'Excel·lència Severo Ochoa des de 2011, és un centre CERCA i membre del Barcelona Institute of Science and Technology (BIST).