Images
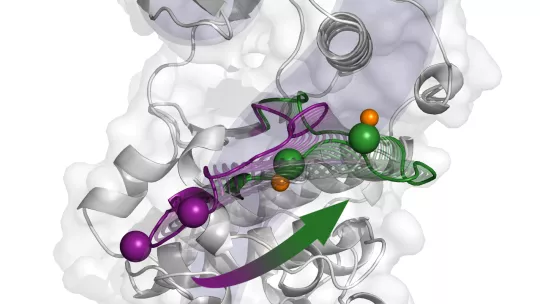
p38α és una proteïna implicada en malalties inflamatòries cròniques i càncer, entre altres condicions patològiques.
Publicat a la revista eLife, l'estudi proporciona una comprensió més profunda de l'estructura de la proteïna, obrint així el camí per al desenvolupament d'inhibidors més eficaços.
Aquest treball és el resultat de la combinació de dades biològiques fonamentals mitjançant tècniques computacionals.
La proteïna p38α és un membre d'una família de molècules que transmeten senyals des de l’exterior a tota la cèl·lula, permetent així una resposta cel·lular apropiada, com la proliferació, diferenciació, senescència o mort. Al mateix temps, la participació de p38α en condicions patològiques, com les malalties inflamatòries cròniques i el càncer, la converteixen en un prometedor objectiu farmacològic. En aquest sentit, una imatge completa del mecanisme d'activació de la proteïna és essencial per dissenyar inhibidors específics que no afectin a altres processos.
La revista eLife ha publicat un estudi sobre p38α realitzat per Antonija Kuzmanic, una investigadora del programa Marie Curie COFUND de la UE, que du a terme una formació postdoctoral simultàniament en dos laboratoris de l'IRB Barcelona: el Laboratori de Modelització Molecular i Bioinformàtica i el Laboratori de Senyalització i Cicle Cel·lular. La col·laboració entre el laboratori encapçalat per Modesto Orozco i l’encapçalat per Angel R. Nebreda, expert de renom mundial en p38α, ha proporcionat una imatge integradora del mecanisme d'activació de p38α i nous coneixements sobre els efectes moleculars de diverses molècules que regulen l'activitat enzimàtica de la proteïna.
Mitjançant tècniques computacionals, els investigadors han desxifrat els elements clau del mecanisme molecular complex subjacent a l'activitat de p38α. Aquest estudi descriu el mecanisme d'activació de la proteïna amb un detall sense precedents i concilia els resultats aparentment contradictoris d'estudis estructurals previs. "Tenint en compte la importància de la proteïna p38α per als processos patològics, esperem que el coneixement obtingut en aquest estudi ajudi a dirigir la proteïna amb més especificitat", destaca Antonija Kuzmanic, autora principal de l'estudi.
Identificant nous inhibidors
p38α ha estat diana de malalties inflamatòries i alguns tipus de càncer. No obstant això, cap fàrmac ha arribat encara al mercat. "El nostre estudi revela noves conformacions de la proteïna, que podrien ser utilitzades com a punt de partida en els estudis de cribratge virtual, amb l'objectiu de descobrir nous inhibidors", explica Kuzmanic. I afegeix: "També hem pogut ressaltar importants interaccions electrostàtiques, el que ens permet explorar rutes alternatives d'activació amb major especificitat".
Un enfocament de biologia computacional
"Fem servir únicament tècniques computacionals. Principalment, hem emprat nombroses simulacions de dinàmica molecular combinades amb una tècnica de mostreig avançada anomenada 'metadinàmica'", explica Kuzmanic. Aquesta combinació dóna als investigadors un avantatge sobre les simulacions estàndard de dinàmica molecular, ja que els permet observar grans canvis conformacionals en una quantitat raonable de temps computacional. A més, "som capaços d'afegir significació estadística a les conformacions que observem en les nostres simulacions".
Aquest estudi ha rebut el suport de Seventh Framework Programme, Engineering and Physical Sciences Research Council, European Research Council, Horizon 2020, i el Ministeri d'Economia, Indústria i Competitivitat (MINECO).
Article de referència:
Antonija Kuzmanic, Ludovico Sutto, Giorgio Saladino, Angel R. Nebreda, Francesco L. Gervasio and Modesto Orozco.
Changes in the free-energy landscape of p38α MAP kinase through its canonical activation and binding events as studied by enhanced molecular dynamics simulations
eLife (2017) DOI: 10.7554/eLife.22175
Sobre l'IRB Barcelona
Creat el 2005 per la Generalitat de Catalunya i la Universitat de Barcelona, l'IRB Barcelona és Centre d'Excel·lència Severo Ochoa des de 2011. El seu objectiu és fer recerca d'excel·lència en biomedicina i millorar la qualitat de vida de les persones i, al mateix temps, tenir cura de la formació de talent, la transferència tecnològica i la comunicació social de la ciència. Els 24 laboratoris i set plataformes tecnològiques treballen per respondre a preguntes bàsiques en biologia i orientades a malalties com ara el càncer, la metàstasi, l’Alzheimer, la diabetis i malalties rares. És un centre internacional que acull més de 400 treballadors de 36 nacionalitats. Està ubicat en el Parc Científic de Barcelona. L’IRB Barcelona forma part del Barcelona Institute of Science and Technology (BIST) i la xarxa de Centres de Recerca de Catalunya (CERCA).
IRB Barcelona
L’Institut de Recerca Biomèdica (IRB Barcelona) treballa per aconseguir una vida lliure de malalties. Desenvolupa una recerca multidisciplinària d’excel·lència per curar el càncer i altres malalties vinculades a l'envelliment. Treballa establint col·laboracions amb la indústria farmacèutica i els principals hospitals per fer arribar els resultats de la recerca a la societat a través de la transferència de tecnologia, i du a terme diferents iniciatives de divulgació científica per mantenir un diàleg obert amb la ciutadania. L’IRB Barcelona és un centre internacional que acull al voltant de 400 investigadors de més de 30 nacionalitats. Reconegut com a Centre d'Excel·lència Severo Ochoa des de 2011, és un centre CERCA i membre del Barcelona Institute of Science and Technology (BIST).