Images
Des de fa vàries dècades, la indústria farmacèutica està interessada en obtenir pèptids anàlegs –molècules similars amb propietats millorades- de l’hormona natural somatostatina. Aquesta hormona i dos compostos anàlegs més -octreotide i lanreotide- s’usen com a fàrmacs en el tractament de diversos tipus de neoplàsies –com el càncer de tiroides, pàncrees o pròstata-, en malalties relacionades amb l’hormona del creixement –per exemple, en el gegantisme- i en hemorràgies digestives. Un equip de científics de l’IRB Barcelona, liderats per Antoni Riera (Universitat de Barcelona) i Maria Macias (Professora de Recerca ICREA), en col·laboració amb l’empresa BCN Peptides, ha dissenyat un pèptid deu vegades més estable en sang que l’hormona natural i més actiu que els dos anàlegs disponibles al mercat. L’èxit del disseny resideix en la substitució de dos residus de la seqüència natural por dos aminoàcids no naturals. Angewandte Chemie, la segona revista de química en índex d’impacte, ha publicat el treball en edició avançada digital i l’ha seleccionat com a destacat per a la portada de l’edició de febrer.
“L’ús de l’hormona natural té dos inconvenients: es degrada ràpidament en l’organisme, entre dos i tres minuts, i té un espectre d’activitat molt ampli. Per això és important desenvolupar compostos més estables en sang i més selectius en la funció quan es pretenen corregir certes malalties sense afectar el normal funcionament de l’hormona natural. El que hem obtingut en el laboratori és un pèptid que compleix amb els dos objectius”, explica Antoni Riera, cap del Laboratori de Síntesi Asimètrica de l’IRB Barcelona on s’ha sintetitzat el nou compost. “A més es podria convertir ràpidament en fàrmac perquè aquests tipus de pèptids no acostumen a tenir problemes de toxicitat”, afegeix l'investigador.
El treball dels doctors Riera i Macias aporta també, per primera vegada, dades estructurals sobre una de les moltes conformacions que té l’hormona somatostatina natural. Aquesta proteïna adapta la seva estructura segons la funció que fa, funció que està determinada per la interacció amb els diferents receptors (en la actualitat se’n coneixen cinc). Les múltiples conformacions impossibiliten l’obtenció d’una única estructura ni en solució ni amb tècniques de difracció de raigs X. “A través de la resolució de l’estructura dels compostos sintetitzats en el laboratori i la seva comparació amb les dades de l’hormona natural”, explica Maria Macias, cap del Laboratori d'Espectroscopia de Ressonància Magnètica Nuclear de Proteïnes, “hem pogut aproximar-nos a la conformació activa de la somatostatina en la interacció amb un dels receptors, en concret el SSTR2”. Per als autors del treball tant la innovació en la síntesi química del compost com la nova aproximació estructural, combinada amb assajos funcionals, permeten un disseny més racional de compostos anàlegs de pèptids naturals i obren noves vies per dissenyar anàlegs que interaccionin amb altres receptors.
El primer signant de l’article és l’estudiant de doctorat de l’IRB Barcelona, Pablo Martín–Gago, i ha involucrat a deu investigadors més, entre els que hi ha tres científics de BCN Peptides SL i tres de la Universitat d’Alcalá de Henares.
Article de referència
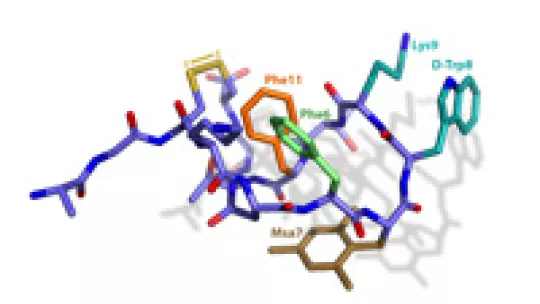
Fine-tuning the π-π Aromatic Interactions in Peptides: Somatostatin Analogues Containing Mesityl Alanine.
Martín-Gago P, Gomez-Caminals M, Ramón R, Verdaguer X, Martin-Malpartida P, Aragón E, Fernández-Carneado J, Ponsati B, López-Ruiz P, Cortes MA, Colás B, Macias MJ, Riera A.
Angew Chem Int Ed Engl. 2012 Jan 5. doi: 10.1002/anie.201108928. [Epub ahead of print]
IRB Barcelona
L’Institut de Recerca Biomèdica (IRB Barcelona) treballa per aconseguir una vida lliure de malalties. Desenvolupa una recerca multidisciplinària d’excel·lència per curar el càncer i altres malalties vinculades a l'envelliment. Treballa establint col·laboracions amb la indústria farmacèutica i els principals hospitals per fer arribar els resultats de la recerca a la societat a través de la transferència de tecnologia, i du a terme diferents iniciatives de divulgació científica per mantenir un diàleg obert amb la ciutadania. L’IRB Barcelona és un centre internacional que acull al voltant de 400 investigadors de més de 30 nacionalitats. Reconegut com a Centre d'Excel·lència Severo Ochoa des de 2011, és un centre CERCA i membre del Barcelona Institute of Science and Technology (BIST).