Images
Científics de l’IRB Barcelona en col·laboració amb investigadors de la Universitat de Barcelona observen que agrupacions d’entre 20 a 100 unitats de beta amiloide adopten una determinada estructura que les fa nocives per a les neurones.
És la primera vegada que una metodologia permet fer un seguiment del procés d’agregació i alhora detectar que un patró estructural és responsable de la toxicitat d´agrupacions de beta amiloide.
Els investigadors diuen que aquests estudis són un pas endavant per trobar una diana terapèutica per a una malaltia, ara per ara, orfe de medicaments.
El pèptid - proteïna petita - beta amiloide està fortament associat a la malaltia d’Alzheimer però encara es busca la prova inequívoca que el situï com la causa principal de l’origen i el desenvolupament de malaltia. El principal escull per confirmar-ho és que la beta amiloide no fa mal quan està sola sinó quan s’agrupa amb ella mateixa fins que forma les anomenades fibres amiloides.
“No tractem amb una única diana, la beta amiloide, sinó que les dianes són múltiples perquè cada agrupació de beta amiloide que es forma durant el procés d’agregació, des de dues unitats fins a 3.000, és una diana potencial. Establir quina d’aquestes agrupacions és responsable de la mort neuronal és un repte complex i és un dels punts crítics per corroborar o refutar la hipòtesi beta amiloide”, explica Natàlia Carulla, investigadora de l’Institut de Recerca Biomèdica (IRB Barcelona), principal responsable de l’estudi que avui publica la revista científica ACS Chemical Biology. En aquest darrer treball, Carulla i col·laboradors presenten la metodologia que ha permès per primera vegada distingir diferents tipus d’agrupacions de beta amiloide durant el procés d’agregació i, en paral·lel, establir quina d’elles és més tòxica. L’estudi aporta més evidències cap a la hipòtesi que la mort de neurones la provoquen els agregats intermedis de beta amiloide i revela que el desenvolupament d’estructura és clau a l’hora de provocar-ne la mort.
Les formes nocives de beta amiloide
El treball demostra que les acumulacions més tòxiques van de grupuscles d’entre 20 a 100 unitats de beta amiloide, el que es coneix com a agregats intermedis o agregats precursors de les fibres beta amiloide. Per contra, per a les formes més petites d’agrupacions de beta amiloide i per a les fibres, que poden incloure fins a 3.000 unitats de pèptid, els investigadors no detecten pràcticament mort neuronal.
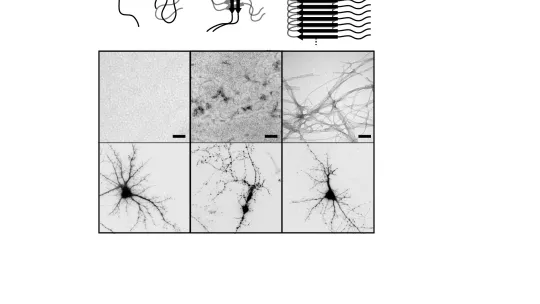
Els científics van tractar neurones de ratolí en cultiu amb mostres d’agregats obtingudes a diferents temps del procés d’agregació. El moment on observaren màxima mortalitat de neurones, vora el 60%, es donava quan hi havia en el cultiu agregats intermedis de beta amiloide que havien desenvolupat un cert grau d’estructura. L’experiment amb neurones de ratolí es va fer en col·laboració amb el laboratori d’Eduardo Soriano de la Universitat de Barcelona, on van preparar cultius de neurones de l’hipocamp, el lloc on primer s’observa la pèrdua de neurones en la malaltia d’Alzheimer.
“La tècnica que hem posat a punt ens permet detectar com va incrementant l’estructura d’aquests agregats, o dit d’una altra manera, com van agafant forma, com es van ordenant. I observem que quan hi ha una certa part rígida dins el cúmul – el que anomenem estructura-, és quan hi ha la màxima toxicitat”, detalla Carulla.
Aquest és precisament un dels resultats més esperançadors de la recerca presentada avui, assenyalen els científics. “L’esperança és que veiem estructura, un ordre, un patró comú i si aconseguim anar delimitant amb més precisió aquest patró estructural serem capaços de buscar i dissenyar molècules terapèutiques que n’evitin la formació o provoquin la seva ruptura”, assenyala el primer autor de l’article Bernat Serra-Vidal, qui va realitzar la seva tesi doctoral fent aquest treball.
També el Parkinson i la diabetis de tipus 2
A més, els investigadors expliquen que les eines per estudiar el procés d’agregació de la beta amiloide es podrien aplicar per estudiar el procés d’agregació d’altres proteïnes que estan relacionades amb malalties com ara el Parkinson, la malaltia de Huntington i la diabetis de tipus 2.
Article de referència:
Hydrogen/Deuterium Exchange-Protected Oligomers Populated during Aβ Fibril Formation Correlate with Neuronal Cell Death
Bernat Serra-Vidal, Lluís Pujadas, Daniela Rossi, Eduardo Soriano, Sergio Madurga, and Natàlia Carulla
ACS Chem. Biol. (2014): dx.doi.org/10.1021/cb500621x
IRB Barcelona
L’Institut de Recerca Biomèdica (IRB Barcelona) treballa per aconseguir una vida lliure de malalties. Desenvolupa una recerca multidisciplinària d’excel·lència per curar el càncer i altres malalties vinculades a l'envelliment. Treballa establint col·laboracions amb la indústria farmacèutica i els principals hospitals per fer arribar els resultats de la recerca a la societat a través de la transferència de tecnologia, i du a terme diferents iniciatives de divulgació científica per mantenir un diàleg obert amb la ciutadania. L’IRB Barcelona és un centre internacional que acull al voltant de 400 investigadors de més de 30 nacionalitats. Reconegut com a Centre d'Excel·lència Severo Ochoa des de 2011, és un centre CERCA i membre del Barcelona Institute of Science and Technology (BIST).