Images
Investigadores del IRB Barcelona localizan una pieza decisiva de la maquinaria que permite a Staphylococcus aureus transferirse genes de resistencia a antibióticos.
Las bacterias S. aureus representan una amenaza letal en hospitales de todo el mundo
Interrumpir la propagación de cepas de bacterias resistentes es una de las estrategias para combatir las infecciones en los hospitales.
La bacteria Staphylococcus aureus mata 11.300 personas cada año sólo en Estados Unidos por infecciones resistentes a los antibióticos, que corresponden a más de la mitad de las muertes provocadas por infecciones de bacterias resistentes gram-positivo en ese país. La alta letalidad le otorga la rapidez que tienen las bacterias en adquirir genes de resistencia a antibióticos. Un estudio del Instituto de Investigación Biomédica (IRB Barcelona), que ha contado con la colaboración del Centro de Investigaciones Biológicas (CIB-CSIC) de Madrid, identifica la pieza clave de la maquinaria que usan las bacterias Staphylococcus aureus para adquirir y transferirse genes que las hacen resistentes a antibióticos. El trabajo se ha publicado esta semana en edición digital avanzada en Proceedings of the National Academic of Sciences (PNAS).
"La lucha contra las bacterias, sobre todo en entornos hospitalarios donde son un problema de primera magnitud, pasa por entender cómo se transfieren los genes para adaptarse rápidamente a entornos cambiantes, como por ejemplo cuando se encuentran con antibióticos nuevos", señala el líder del estudio y científico del IRB Barcelona Miquel Coll, también investigador del CSIC, que estudia la transferencia horizontal de genes desde la biología estructural.
Impedir la propagación
"Una habilidad extraordinaria de las bacterias para evolucionar y adaptarse rápidamente es esta transferencia horizontal de genes, que los humanos por ejemplo no tenemos", explica Coll. Una de estas vías se llama conjugación: dos bacterias se unen para pasarse un fragmento de ADN, llamado plásmido. "Un plásmido es un trozo pequeño de ADN en forma de círculo que contiene muy pocos genes, donde se localizan normalmente genes selectivos de resistencia a antibióticos, y que tardan sólo unos minutos a ser transferidos entre bacterias", detalla.
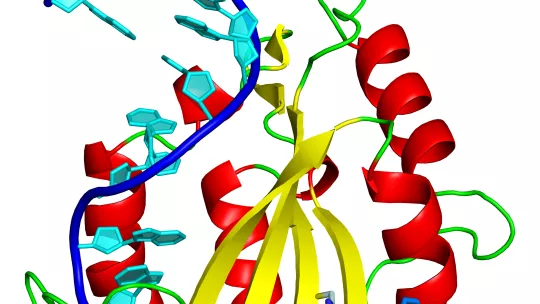
En la transferencia horizontal interviene una maquinaria donde la relaxasa, una proteína enzimática, es una pieza clave. Gracias a la resolución de la estructura en tres dimensiones del complejo que forma la relaxasa con el ADN del plásmido, los investigadores han identificado un aminoácido, una histidina, como el elemento central para que se produzca la transferencia y se propague la resistencia.
"Lo que es nuevo es que la relaxasa de diferentes cepas de Staphylococcus aureus es especial porque usa un aminoácido que no se había visto nunca en ningún otra de las relaxasas que conocemos", precisa el primer firmante del estudio, Radoslaw Pluta, estudiante de doctorado de "la Caixa" en el IRB Barcelona, y actualmente investigador postdoctoral en el International Institute of Molecular and Cell Biology en Varsovia, Polonia.
La histidina es el residuo catalítico que permite a la relaxasa cortar el ADN, unirse a él, estirar una de las dos cadenas y llevársela para traspasarla a la bacteria receptora, donde la cadena se replicará para formar, de nuevo, la doble cadena del plásmido. Este nuevo plásmido ya contendrá los genes de resistencia y la maquinaria para transferirlos a otra bacteria. Los científicos informan que esta histidina catalítica está presente en las relaxasas del 85% de cepas de Staphylococcus aureus.
Para comprobar que la histidina es decisiva, los investigadores del grupo de Manuel Espinosa del CIB-CSIC, que han participado en el estudio, la intercambiaron por un aminoácido diferente y confirmaron en placas con cultivos que se impedía la transferencia.
La mutación de la histidina no mata la bacteria sólo impide la transferencia de genes. ¿Como se podría usar esto para combatir las infecciones? "No lo sé", admite Coll, "pero ahora sabemos más detalles de una bacteria letal y por lo tanto nos podría conducir a desarrollar moléculas para evitar la propagación de cepas resistentes".
Coll explica que las infecciones hospitalarias son las más difíciles de combatir. "Ahora mismo estamos como en una carrera que siempre perdemos porque cuando se usa un antibiótico diferente enseguida aparecen resistencias y se propagan", describe. El científico añade que el arsenal de antibióticos en reserva de los hospitales para tratar las infecciones resistentes es "demasiado" corto. Aparte de la dificultad de generar nuevos antibióticos, Coll también resalta como escollo para avanzar más rápidamente que "haya poca inversión, ya que la industria muestra otras prioridades. Esto es legítimo, por eso hay que sumar inversiones de fondos públicos y privados ".
En este trabajo ha colaborado el grupo de Modesto Orozco, también en el IRB Barcelona, que ha proporcionado el estudio teórico que otorga validez a la reacción química entre el ADN del plásmido y la proteína a través de la histidina. La resolución de la estructura del complejo formado por la proteína y la cadena de ADN se ha realizado con datos obtenidos por difracción de rayos X en el sincrotrón europeo de Grenoble.
Artículo de referencia:
Radoslaw Pluta, D. Roeland Boer, Fabián Lorenzo-Díaz, Silvia Russi, Hansel Gómez, Cris Fernández-López, Rosa Pérez-Luque, Modesto Orozco, Manuel Espinosa and Miquel Coll
PNAS (2017): doi: 10.1073/pnas.1702971114
Sobre el IRB Barcelona
Creado en 2005 por la Generalitat de Catalunya y la Universidad de Barcelona, el IRB Barcelona es Centro de Excelencia Severo Ochoa desde 2011. El objetivo del IRB Barcelona es hacer investigación de excelencia en biomedicina y mejorar la calidad de vida de las personas y, en paralelo, potenciar la formación de talento, la transferencia tecnológica y la comunicación social de la ciencia. Los 25 laboratorios y siete plataformas tecnológicas trabajan para responder a preguntas básicas en biología y orientadas a enfermedades como el cáncer, la metástasis, el Alzheimer, la diabetes y enfermedades raras. Es un centro internacional que acoge alrededor de 400 trabajadores de 32 nacionalidades. Está ubicado en el Parque Científico de Barcelona. El IRB Barcelona forma parte del Barcelona Institute of Science and Technology (BIST) y la red de Centros de Investigación de Catalunya (CERCA).
IRB Barcelona
El Instituto de Investigación Biomédica (IRB Barcelona) trabaja para conseguir una vida libre de enfermedades. Desarrolla una investigación multidisciplinar de excelencia para curar el cáncer y otras enfermedades vinculadas al envejecimiento. Establece colaboraciones con la industria farmacéutica y los principales hospitales para hacer llegar los resultados de la investigación a la sociedad, a través de la transferencia de tecnología, y realiza diferentes iniciativas de divulgación científica para mantener un diálogo abierto con la ciudadanía. El IRB Barcelona es un centro internacional que acoge alrededor de 400 científicos de más de 30 nacionalidades. Reconocido como Centro de Excelencia Severo Ochoa desde 2011, es un centro CERCA y miembro del Barcelona Institute of Science and Technology (BIST).