Images
- Un estudi liderat per l'Institut de Biologia Molecular de Barcelona del CSIC i l'IRB Barcelona revela com el bacteri que causa el còlera activa el seu programa de virulència i descobreix un únic aminoàcid com a punt de contacte crític.
- Mitjançant criomicroscòpia electrònica, els investigadors han resolt cinc estructures de complexos d'activació de V. cholerae, revelant com s'activa l'expressió gènica de virulència una vegada que el bacteri arriba a l'intestí humà.
- Els investigadors de l'IBMB-CSIC i l'IRB Barcelona, en col·laboració amb EMBL Heidelberg i socis als Estats Units, han cartografiat el procés d'infecció amb un detall sense precedents, el que obre noves vies per a futures teràpies.
El còlera continua sent un gran desafiament global de salut pública, amb una estimació anual d'entre 1,3 i 4 milions de casos i desenes de milers de morts reportades a tot el món. Causada pel bacteri Vibrio cholerae, la malaltia es propaga principalment a través d'aigua i aliments contaminats i segueix afectant de forma desproporcionada regions amb accés limitat a sanejament segur.
Els conflictes armats, l'impacte climàtic i el desplaçament poblacional estan provocant un augment de brots epidèmics de còlera. En resposta al recent ressorgiment global de casos, que afecta ja 43 països, i la mortalitat associada (en particular, l'alta mortalitat infantil) l'OMS (Organització Mundial de la Salut) va classificar el còlera com una emergència de grau 3, el seu nivell més alt d'alerta, el 2023.
En un estudi publicat a Science Advances, una col·laboració internacional entre l 'Institut de Biologia Molecular de Barcelona del CSIC, l 'IRB Barcelona, l 'EMBL Heidelberg i la Universitat de Detroit Mercy ofereix una explicació estructural, llargament cercada, de la cascada de mecanismes que permet a Vibrio cholerae colonitzar l'intestí humà i produir la toxina del còlera que causa diarrea potencialment mortal.
ToxR i TcpP són factors de transcripció clau de Vibrio cholerae que detecten senyals externs, com la presència de sals biliars i baixos nivells d'oxigen, a l'intestí prim humà. Un cop activats, s'uneixen a l'ADN bacterià per desencadenar una cascada regulatòria, que condueix a la producció de la toxina del còlera i del pilus corregulat per toxines. Aquest últim és una estructura filamentosa a la superfície del bacteri, que li serveix d'ancoratge per adherir-se a les parets intestinals.
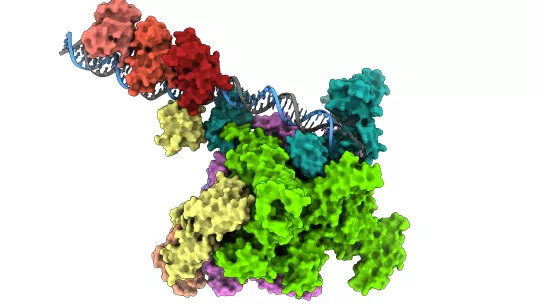
Tot i que aquestes proteïnes, ToxR i TcpP, van ser identificades fa temps com els principals reguladors de la infecció, el mapa 3D de com interactuen amb el motor de transcripció de la cèl·lula bacteriana, l'ARN polimerasa (RNAP), es desconeixia. Ara, aquest nou estudi revela l'arquitectura molecular d'aquesta interacció. Utilitzant criomicroscòpia electrònica (crio-EM), els investigadors demostren que el mecanisme no és el que els científics esperaven.
"Comprendre aquesta interacció a nivell molecular ens dona una nova visió de com es controla la virulència bacteriana", diu el Dr. Miquel Coll, professor d’investigació del CSIC i ex cap de grup del laboratori de Biologia Estructural de Complexos de Proteïnes i Àcids Nucleics i Màquines Moleculars de l'IRB Barcelona.
Estabilitzar la maquinària de transcripció en lloc de remodelar-la
Tot i que molts reguladors bacterians estan dissenyats per forçar un canvi de forma a la polimerasa per iniciar la transcripció, aquest estudi revela que ToxR i TcpP no indueixen cap reajustament conformacional sinó que actuen com a àncores moleculars, estabilitzant una part específica de l'enzim (el domini alfa-CTD) directament sobre l'ADN. Aquestes troballes mostren que l'activació del gen de virulència no s'aconsegueix remodelant la maquinària de transcripció, sinó estabilitzant-la en una configuració productiva.
L'equip va identificar un únic aminoàcid, una fenilalanina, com el pont molecular crític entre el factor de transcripció i la polimerasa. "Si només es muta aquest aminoàcid, tot el procés d'activació falla, fent que els bacteris siguin inofensius", afirma el Dr. Adrià Alcaide, primer autor de l'estudi i investigador de l'IBMB-CSIC.
Implicacions per a futures teràpies
El còlera pot causar una deshidratació mortal en poques hores, especialment en nens i gent gran. Un tractament ràpid amb teràpia de rehidratació i antibiòtics pot reduir significativament la taxa de mortalitat. La similitud molecular observada en aquest estudi entre els llocs actius (on ocorre la transcripció de l'ADN a l'ARN) de l'ARN polimerasa de V. cholerae i E. coli suggereix que els antibiòtics existents que actuen contra la polimerasa bacteriana podrien ser reutilitzats o bé optimitzats per tractar el còlera.
Article de referència:
Structures of Vibrio cholerae transcription complexes reveal how ToxR and TcpP recruit the RNA polymerase and activate virulence genes
Adrià Alcaide-Jiménez, Albert Canals, Florence Baudin, Cristina Machón, Montserrat Fàbrega-Ferrer, Olga Bantysh, Rosa Pérez-Luque, Brice Murciano, Ali A. Mohammad, Michael J. Rowse, Joseph M. Ferracciolo, Eric S. Krukonis, Christoph W. Müller & Miquel Coll
Science Advances (2026) DOI: 10.1126/sciadv.adx9680
IRB Barcelona
L’Institut de Recerca Biomèdica (IRB Barcelona) treballa per aconseguir una vida lliure de malalties. Desenvolupa una recerca multidisciplinària d’excel·lència per curar el càncer i altres malalties vinculades a l'envelliment. Treballa establint col·laboracions amb la indústria farmacèutica i els principals hospitals per fer arribar els resultats de la recerca a la societat a través de la transferència de tecnologia, i du a terme diferents iniciatives de divulgació científica per mantenir un diàleg obert amb la ciutadania. L’IRB Barcelona és un centre internacional que acull al voltant de 400 investigadors de més de 30 nacionalitats. Reconegut com a Centre d'Excel·lència Severo Ochoa des de 2011, és un centre CERCA i membre del Barcelona Institute of Science and Technology (BIST).