Images
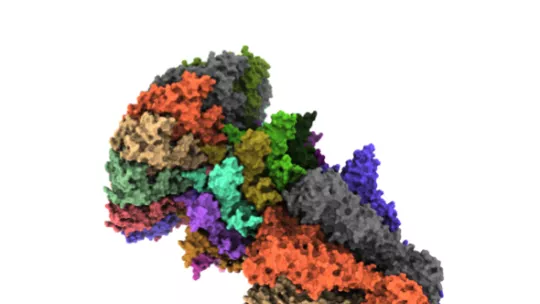
L'estudi revela el model d'obertura i tancament de la proteïna portal durant el procés de maduració de la càpsida viral, on el virus incorpora el seu material genètic.
Els investigadors han emprat una combinació de tècniques de criomicroscòpia i cristal·lografia per estudiar aquests virus que infecten bacteris
Un estudi amb participació del Consell Superior d'Investigacions Científiques (CSIC) i l'Institut de Recerca Biomèdica (IRB Barcelona) ha desxifrat l'estructura i el mecanisme d'actuació d'un complex clau en la infecció del virus bacteriòfag T7. Els resultats es publiquen a la revista Nature Communications.
El treball és fruit de la col·laboració d'experts en criomicroscopía electrònica del Centre Nacional de Biotecnologia (CSIC), dirigits per José L. Carrascosa, i en cristal·lografia de raigs X de l'Institut de Recerca Biomèdica (IRB Barcelona) i l'Institut de Biologia Molecular de Barcelona (CSIC), dirigits per Miquel Coll. Els diferents grups d'investigació han treballat de manera conjunta per combinar els resultats de les dues tècniques, obtenint noves dades sobre el mecanisme d'actuació d'aquesta proteïna en el procés de maduració viral.
"Els bacteriòfags són virus que infecten bacteris. A més del seu interès com a model d'estudi per la seva simplicitat genètica però gran complexitat estructural, ara mateix són un nou focus d'atenció per als investigadors donat el seu potencial com a alternativa a l'ús d'antibiòtics", explica José L. Carrascosa, investigador del Centre Nacional de Biotecnologia i codirector del treball.
Durant el cicle del bacteriòfag T7 es forma una càpsida viral on el virus necessita incloure el seu material genètic, introduint a través d'un petit canal d'entrada format per la proteïna portal que posteriorment es tanca amb la proteïna de la cua del virus. Fins ara es desconeixia quin era el mecanisme que permetia obrir i tancar aquesta "porta" d'entrada de manera controlada.
"Aquests virus bacterians tenen un mecanisme per empaquetar el seu ADN similar als dels virus herpes que infecten humans. Per això, desxifrar com funcionen ajuda a entendre com actuen virus patògens que ens afecten", indica Miquel Coll, investigador de l'IRB Barcelona i de l'Institut de Biologia Molecular de Barcelona i codirector de l'estudi.
Ana Cuervo, investigadora del Centre Nacional de Biotecnologia, i Montserrat Fàbrega-Ferrer, de l'IRB Barcelona i de l'Institut de Biologia Molecular de Barcelona, primeres autores del treball, destaquen com "combinant criomicroscopía electrònica i cristal·lografia de raigs X de sincrotró ens ha permès no només resoldre l'estructura atòmica d'un complex de grans dimensions, fet que suposa un desafiament tècnic, sinó també definir un model d'obertura i tancament del portal durant el procés de maduració de la càpsida viral". D'aquesta manera, els científics han pogut identificar quines són les interaccions entre les diferents proteïnes que permeten els canvis en la conformació del complex, des d'una estructura oberta per permetre el pas de l'ADN viral a una tancada en formar les partícules virals madures.
L’estudi ha comptat amb finançament dels programes d'excel·lència "Severo Ochoa" i “María de Maeztu”, el programa “Ramón y Cajal” del Ministeri de Ciència, Innovació i Universitats, i els projectes europeus iNEXT i Instruct-ERIC.
Article de referència
Ana Cuervo, Montserrat Fàbrega-Ferrer, Cristina Machón, José Javier Conesa, José Javier Fernández, Rosa Pérez-Luque, Mar Pérez-Ruiz, Joan Pous, María Cristina Vega, José L. Carrascosa y Miquel Coll.
Structures of T7 bacteriophage portal and tail suggest a viral DNA retention and ejection mechanism.
Nature Communications (2019) DOI: 10.1038/s41467-019-11705-9
Font: CSIC
IRB Barcelona
L’Institut de Recerca Biomèdica (IRB Barcelona) treballa per aconseguir una vida lliure de malalties. Desenvolupa una recerca multidisciplinària d’excel·lència per curar el càncer i altres malalties vinculades a l'envelliment. Treballa establint col·laboracions amb la indústria farmacèutica i els principals hospitals per fer arribar els resultats de la recerca a la societat a través de la transferència de tecnologia, i du a terme diferents iniciatives de divulgació científica per mantenir un diàleg obert amb la ciutadania. L’IRB Barcelona és un centre internacional que acull al voltant de 400 investigadors de més de 30 nacionalitats. Reconegut com a Centre d'Excel·lència Severo Ochoa des de 2011, és un centre CERCA i membre del Barcelona Institute of Science and Technology (BIST).