Images
Un estudi de l'IRB Barcelona en càncer de mama identifica la proteïna p38 com un salvavides que fan servir les cèl·lules tumorals per evitar dany excessiu en el seu ADN que, d'una altra manera, les sentenciaria a morir.
Bloquejant p38 aconsegueixen elevar la mortalitat de cèl·lules tumorals i reduir els tumors.
La combinació d'inhibidors de p38 amb medicaments de quimioteràpia (taxans), potència, accelera o allarga l'efecte antitumoral en tumors de pacients crescuts en ratolins.
Conèixer al detall els mecanismes que contribueixen a la supervivència de les cèl·lules tumorals ajuda a desarmar-los. La investigació publicada avui a la revista Cancer Cell, liderada per l'investigador ICREA de l'Institut de Recerca Biomèdica (IRB Barcelona), Angel R. Nebreda, revela un nou mecanisme protector de les cèl·lules tumorals en càncer de mama i assenyala noves dianes terapèutiques per tractar-lo. L'estudi ha estat possible gràcies a dos ajuts competitius del Consell Europeu de Recerca, ERC Advanced i ERC Proof of Concept.
Els resultats demostren que la proteïna p38alfa (p38 d’ara endavant) actua com a protector de les cèl·lules tumorals perquè està implicada en encendre un mecanisme de reparació de l'ADN. D'aquesta manera, p38 salva les cèl·lules tumorals de sucumbir per acumulació excessiva d'errors, o mutacions, en el seu ADN. "De forma inherent les cèl·lules tumorals tendeixen a acumular dany en l'ADN però algunes n’acumulen més que d’altres i veiem que aquestes són les que depenen més de l'acció de p38", explica Nebreda.
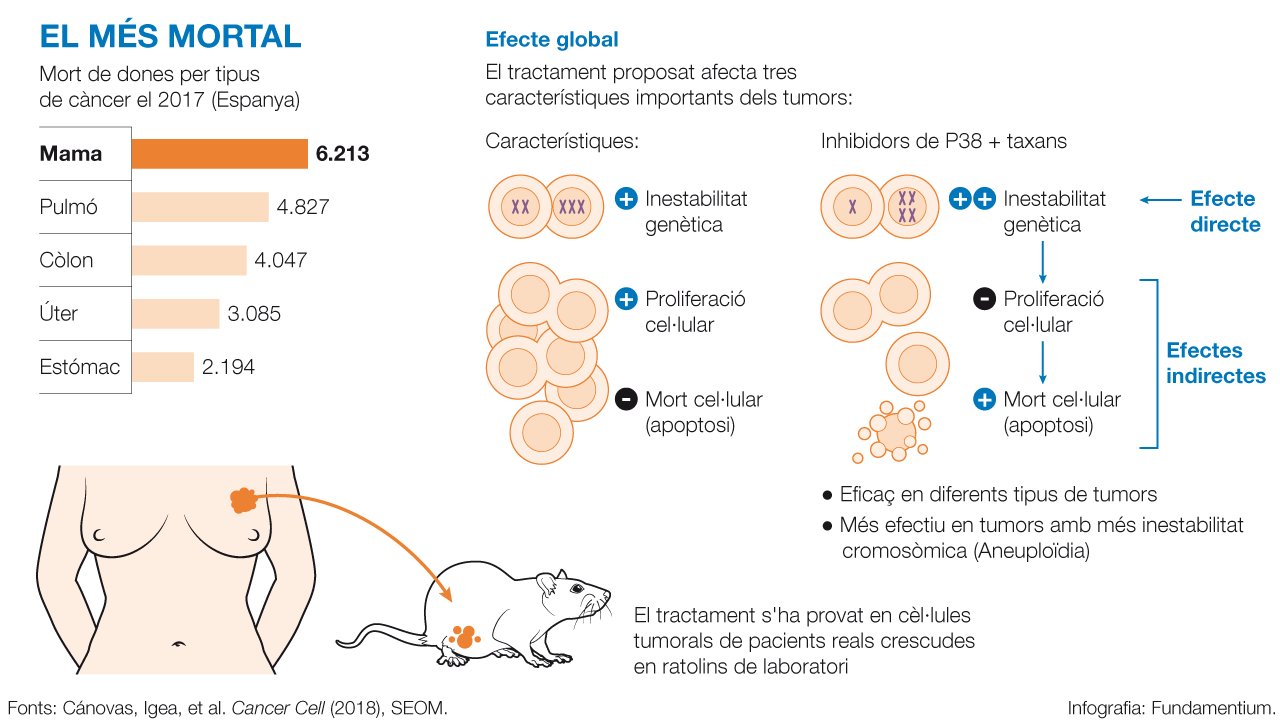
El càncer de mama és, en dones, el tumor més mortífer al món -521.000 morts a l'any-, així com a Espanya -6.213 anuals- (fonts: Organització Mundial de la Salut 2012 i SEOM 2017).
Existeixen, principalment, tres tipus de càncer de mama: el receptor d'estrogen positiu (ER), el HER 2 positiu i el triple negatiu. Els experiments es van fer en un model que desenvolupa tumors de mama triple negatiu. Aquest tipus de tumor suposa el 15% de casos de càncer de mama i l'única opció terapèutica coneguda, fins ara, és la quimioteràpia genèrica, mentre que per als altres dos tipus hi ha teràpies dirigides. Aquests descobriments podrien obrir la porta a millorar el tractament per al tumor de mama triple negatiu.
Bloquejar p38 per optimitzar la quimioteràpia
Els investigadors van usar fàrmacs inhibidors de p38 per bloquejar-ne l'acció en cèl·lules tumorals. Aquests inhibidors ja han estat utilitzats en assajos clínics amb pacients, però per a altres malalties. Els inhibidors de p38 es van combinar amb medicaments de quimioteràpia clàssica denominats taxans, com el paclitaxel i el docetaxel. Com preveien, les cèl·lules tumorals tractades amb la teràpia combinada acumulaven més inestabilitat cromosòmica, és a dir, més dany en el seu ADN així com variacions en el nombre de cromosomes, de manera que moltes morien i es reduïa considerablement la massa tumoral.
Es van utilitzar 9 tumors de pacients crescuts en ratolins. En set d'ells, incloent tant ER com triple negatiu, l'inhibidor de p38 va potenciar, accelerar o allargar l'efecte antitumoral dels taxans.
"Els taxans impedeixen la divisió cel·lular danyant els cromosomes i generant inestabilitat cromosòmica. Com intuíem, atès que p38 actua com un fre a aquesta acció, quan la inhabilitem les cèl·lules es queden sense la protecció i els taxans actuen més eficaçment", explica Begoña Cánovas, estudiant de doctorat de "la Caixa" i primera autora de l'article juntament Ana Igea, investigadora postdoctoral i avui Alumni de l'IRB Barcelona a la Universitat de Vigo.
Pacients seleccionats
Els investigadors creuen haver trobat, a més, una possible explicació de per què dos dels tumors analitzats no responien a la teràpia, el que podria permetre distingir a les pacients que podrien beneficiar-se’n de les que no. Van veure que l'eficiència del tractament depenia del grau d'inestabilitat cromosòmica de les cèl·lules tumorals: a més inestabilitat, millor funciona la teràpia.
"Des del punt de vista de l'aplicació, és un dels resultats més interessants d'aquest estudi ja que hi ha maneres senzilles de mesurar el grau d'inestabilitat cromosòmica dels tumors. Però també és cert que necessitem confirmar-ho amb un major nombre de tumors de pacients ", adverteix Nebreda.
"Esperem que es facin aquests estudis, en col·laboració amb nosaltres o en altres laboratoris, i que de validar-se, la indústria farmacèutica s'interessi per dur a terme els assajos per comprovar l'eficiència del tractament combinat amb pacients reals", afegeix.
A més del finançament del Consell Europeu de Recerca, l’estudi ha comptat amb el suport del Ministeri d’Economia i Competitivitat, la Generalitat de Catalunya i la Fundació BBVA. El treball s’ha fet en col·laboració amb Roger Gomis, especialista en càncer de mama, i Travis Stracker, especialista en inestabilitat genòmica, ambdós a l’IRB Barcelona: ; Eva Gonzalez-Suarez i Violeta Serra de l’IDIBELL i el VHIO, respectivament, de Barcelona; la Universitat de Zurich, a Suïssa, i la Universitat d’Austin, als Estats Units.
L'article publicat per científics de l'IRB Barcelona a Cancer Cell identifica la funció de la proteïna p38 en el desenvolupament de càncer de mama i proposa noves vies de tractament.
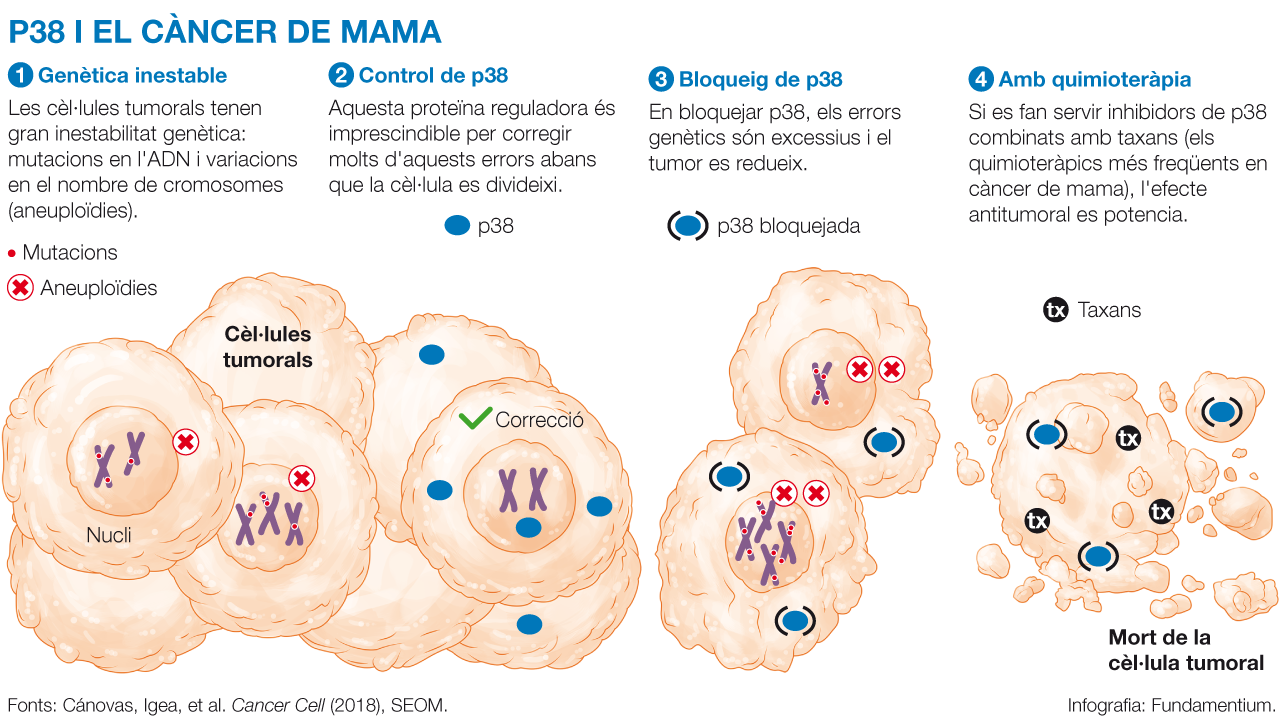
1. Genètica inestable
Les cèl·lules tumorals tenen gran inestabilitat genètica: mutacions en l'ADN i variacions en el nombre de cromosomes (aneuploïdies).

2. Control de p38
Aquesta proteïna reguladora és imprescindible per corregir molts d'aquests errors abans que la cèl·lula es divideixi.

3. Bloqueig de p38
En bloquejar p38, els errors genètics són excessius i el tumor es redueix.
 <
<
4. Combinació amb quimioteràpia
Si es fan servir inhibidors de p38 combinats amb taxans (els quimioteràpics més freqüents en càncer de mama), l'efecte antitumoral es potencia.

Efecte global
El tractament proposat afecta tres característiques importants dels tumors:

El tractament s'ha provat en cèl·lules tumorals de pacients reals crescudes en ratolins de laboratori
- Eficaç en diferents tipus de tumors
- Més efectiu en tumors amb més inestabilitat cromosòmica (Aneuploïdia)

El més mortal
Mort de dones per tipus de càncer el 2017 (Espanya)

Fonts: Cánovas, Igea, et al. Cancer Cell (2018), SEOM.
Infografia: Fundamentium.
Article de referència:
Begoña Cánovas, Ana Igea, Alessandro A. Sartori, Roger R. Gomis, Tanya T. Paull, Michitaka Isoda, Héctor Perez-Montoyo, Violeta Serra, Eva González-Suárez, Travis H. Stracker and Angel R. Nebreda
Targeting p38a increases DNA damage, chromosome instability and the anti-tumoral response to taxanes in breast cancer cells
Cancer Cell (2018): doi: 10.1016/j.ccell.2018.04.010
IRB Barcelona
L’Institut de Recerca Biomèdica (IRB Barcelona) treballa per aconseguir una vida lliure de malalties. Desenvolupa una recerca multidisciplinària d’excel·lència per curar el càncer i altres malalties vinculades a l'envelliment. Treballa establint col·laboracions amb la indústria farmacèutica i els principals hospitals per fer arribar els resultats de la recerca a la societat a través de la transferència de tecnologia, i du a terme diferents iniciatives de divulgació científica per mantenir un diàleg obert amb la ciutadania. L’IRB Barcelona és un centre internacional que acull al voltant de 400 investigadors de més de 30 nacionalitats. Reconegut com a Centre d'Excel·lència Severo Ochoa des de 2011, és un centre CERCA i membre del Barcelona Institute of Science and Technology (BIST).