Images
Para la comunidad científica, la proteína POP (prolil oligopeptidasa) es un objetivo terapéutico para el tratamiento de desórdenes cognitivos y neurodegenerativos.
Investigadores del IRB Barcelona consiguen los primeros inhibidores de POP irreversibles, selectivos y permeables al cerebro.
Un artículo publicado por investigadores del Instituto de Investigación Biomédica (IRB Barcelona) en Cell Chemical Biology describe una nueva clase de inhibidores para la proteína POP (prolil oligopeptidasa). Esta proteína se encuentra presente principalmente en el cerebro y es un objetivo terapéutico "atractivo" para el tratamiento de varios desórdenes cognitivos y neurodegenerativos, como la enfermedad de Parkinson y la esquizofrenia.
La mayoría de los inhibidores de POP desarrollados hasta ahora duran poco en la sangre, no son suficientemente selectivos para la proteína y no consiguen cruzar la barrera hematoencefálica (que protege el cerebro), lo que ha limitado su potencial como fármaco.
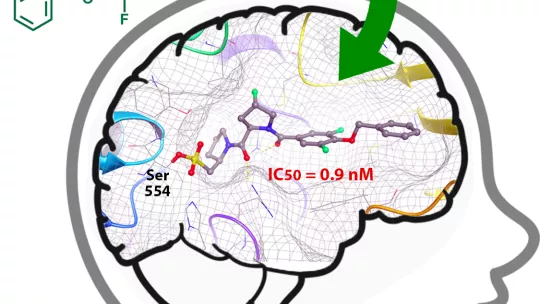
El trabajo del investigador postdoctoral del IRB Barcelona, Salvador Guardiola, describe los primeros inhibidores de POP duraderos, selectivos y con las propiedades adecuadas para acceder al cerebro. En el laboratorio de Diseño, Síntesis y Estructura de Péptidos y Proteínas, liderado por Ernest Giralt, han generado y caracterizado una familia de 15 péptidos (proteínas pequeñas) modificados, llamados peptidomiméticos, con resultados prometedores.
"Los péptidos naturales son poco estables en tejidos y tienen actividades relativamente débiles. En cambio, si los modificamos con aminoácidos no naturales e introducimos grupos funcionales diseñados para reaccionar con la diana terapéutica, podemos conseguir péptidos mucho más activos y eficaces", explica Guardiola.
A concentraciones bajas, estos nuevos péptidos producen una inhibición rápida, específica y sostenida de POP, tanto en la enzima aislada como en células humanas intactas. Además, son altamente selectivos con dos proteasas muy parecidas a POP (DPPIV y FAP) y muestran una alta permeabilidad de la barrera hematoencefálica, describen los investigadores.
"Con estos inhibidores abrimos la puerta a que se desarrollen nuevos tratamientos para las patologías del sistema nervioso central, además de poder aplicarse para estudiar la función de POP en estos trastornos y diseñar inhibidores para otras proteasas", destaca el científico del IRB Barcelona Ernest Giralt, también catedrático de la Universidad de Barcelona.
Este estudio ha sido financiado por el Ministerio de Economía y Competitividad y fondos FEDER y por la Generalitat de Catalunya. Ha contribuido la Unidad de Resonancia Magnética Nuclear de la UB, la plataforma de Espectrometría de Masas y Proteómica del IRB Barcelona y el Barcelona Supercomputing Center. El trabajo se ha realizado en colaboración con científicos de la Universidad de Glasgow (Escocia, Gran Bretaña), del Utrecht Institute for Pharmaceutical Sciences (Holanda) y la empresa biotecnológica Iproteos, spin off del IRB Barcelona y la Universidad de Barcelona.
Vídeo sobre la investigación de Ernest Giralt: "The power of the medicinal chemistry" - Meet Our Scientists
Artículo de referencia:
Salvador Guardiola, Roger Prades, Laura Mendieta, Arwin J. Brouwer, Jelle Streefkerk, Laura Nevola, Teresa Tarragó, Rob M. J. Liskamp, Ernest Giralt
Targeted covalent inhibition of prolyl oligopeptidase (POP): discovery of sulfonylfluoride peptidomimetics
Cell Chemical Biology (2018) DOI: 10.1016/j.chembiol.2018.04.013
IRB Barcelona
El Instituto de Investigación Biomédica (IRB Barcelona) trabaja para conseguir una vida libre de enfermedades. Desarrolla una investigación multidisciplinar de excelencia para curar el cáncer y otras enfermedades vinculadas al envejecimiento. Establece colaboraciones con la industria farmacéutica y los principales hospitales para hacer llegar los resultados de la investigación a la sociedad, a través de la transferencia de tecnología, y realiza diferentes iniciativas de divulgación científica para mantener un diálogo abierto con la ciudadanía. El IRB Barcelona es un centro internacional que acoge alrededor de 400 científicos de más de 30 nacionalidades. Reconocido como Centro de Excelencia Severo Ochoa desde 2011, es un centro CERCA y miembro del Barcelona Institute of Science and Technology (BIST).